- +1
你的預測,如何影響你的時間感知?| Paper Alert
原創 NR 神經前研 來自專輯Paper Alert
認知與行為
果蠅能看到視覺錯覺嗎?
Agrochao et al., PNAS
人類能從靜態的鋸齒形梯度圖案(stationary sawtooth gradients,下圖A)中感知到運動,這被稱為“運動視覺”(illusory motion)。近日,來自耶魯大學的新研究發現,果蠅也能夠感知到運動視覺,該感知由運動檢測神經元(motion detector neuron)T4和T5參與。在感知到運動時,果蠅會立即將身體朝著感知到的運動方向(optomotor turning)轉動。研究人員在向果蠅呈現該圖片后,果蠅轉動的方向與人類感知的錯覺方向一致(下圖B、C)。
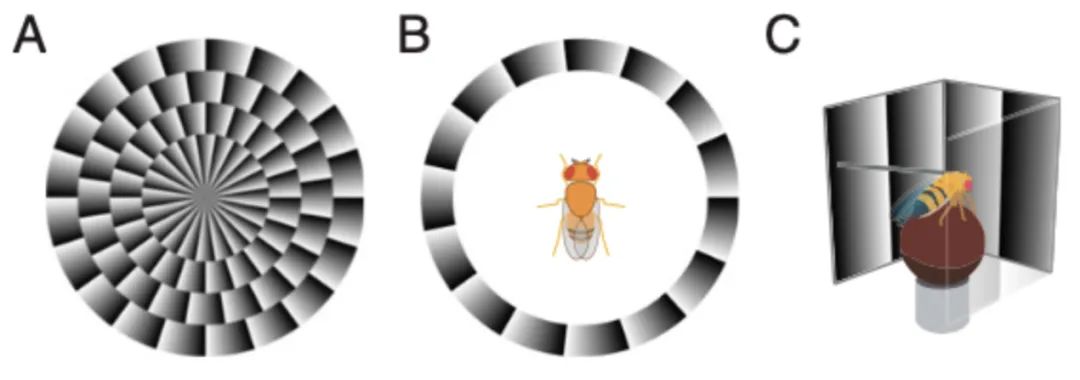
研究人員探究了T4和T5神經元引發這種行為的機制。通過抑制(silence)這兩種神經元,他們成功改變了果蠅對于運動視覺的感知——當同時抑制T4與T5時,果蠅感知到的錯覺似乎消失了;而當僅僅抑制其中一種神經元時,果蠅似乎感知到了方向相反的運動視覺。
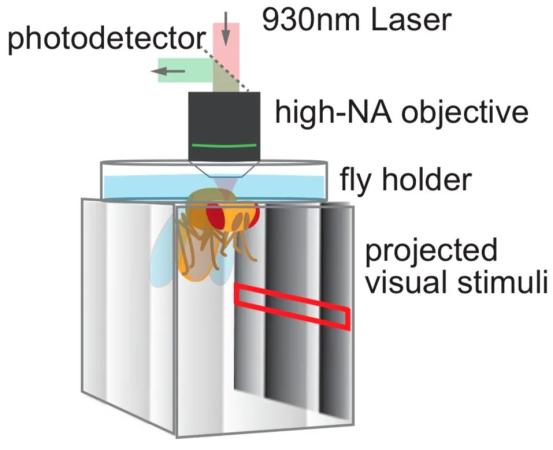
該研究顯示,果蠅之所以在觀看靜態梯度圖片時感知到了運動視覺,是由于它們的運動檢測神經元T4和T5沒有及時取消其對圖片中的對比邊緣的響應。此外,他們還探究了同一范式中的人類反應,結果顯示人類對該錯覺的加工,與果蠅的加工機制類似。
doi: 10.1073/pnas.2002937117
參考文章:https://www.sciencedaily.com/releases/2020/08/200824170451.htm
大鼠,不只是大:
大小鼠之間的物種差異揭示
調控父愛行為的神經-激素環路
Stagkourakis et al., Cell
照顧子代是物種進化過程中十分重要的行為。有趣的是,父愛行為在進化過程中出現了明顯的物種差異,即使是在進化樹上位置十分相近的大鼠(Sprague-Dawley rat)與小鼠(野生型C57BL/6J),也表現出了完全相反的行為模式:小鼠父親會展現出照顧子代的行為,而大鼠父親則對子代不聞不問。研究團隊基于先前發現的雄性大小鼠之間,位于下丘腦背中部弓狀核(dorsomedial arcuate nucleus of the hypothalamus,dmArc)的結節漏斗部多巴胺能神經元(tuberoinfundibular dopamine neurons,TIDA neurons)的活性差異,進一步探究其與跨物種行為差異之間的關聯與可能的調控機制。
研究人員通過注射催乳素(prolactin,PRL)以及敲除在內側視交叉前區(medial preoptic area,mPOA)中的催乳素受體基因,表明了催乳素對于內側視交叉前區神經元的直接調控作用。接著,他們通過使用不同頻率的體外光刺激,改變TIDA神經元的發放頻率,揭示了其與催產素水平之間的因果關系。這些結果表明,TIDA-PRL環路參與了父愛行為的調控。
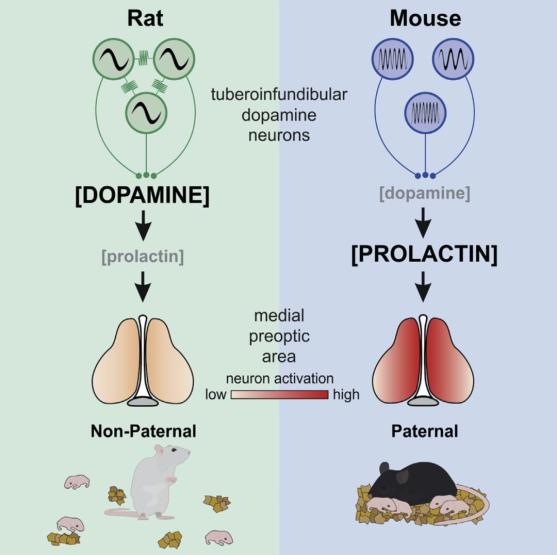
值得注意的是,這條環路的形成似乎與雄鼠的過往性經歷沒有關聯,而過往的研究發現有性經歷的雄鼠會展現出更多的照顧子代的行為。因此,這篇文章中發現的調控父愛行為的環路,可能并不是參與行為調控的唯一環路。
doi: 10.1073/pnas.1922401117
人類決策中的概率失真
Zhang et al., PNAS
空難發生的概率很低,但不少人仍然害怕坐飛機;兒童注射疫苗帶來危害的可能性更是微乎其微,但疫苗有害論仍在社交網站上盛行。人類表征外界信息時總會出現這樣的概率失真(probability distortion)。一項來自紐約大學及北京大學的近期研究探究了概率失真的一般機制。他們認為,概率失真是人類彌補自身認知局限(cognitive limitation)的策略。
該研究團隊提出了有界邏輯變換模型(bounded log-odds model,BLO)。該模型的一個重要因素是人腦如何對客觀概率進行重編碼——他們認為,這與客觀概率的范圍(range)相關。舉個例子,出現空難的概率極低,該概率的范圍也就很低。對于這樣的客觀概率,人們會透過“認知放大鏡”對其進行重編碼,這也就導致了人們主觀認知上的空難比實際情況嚴重得多。
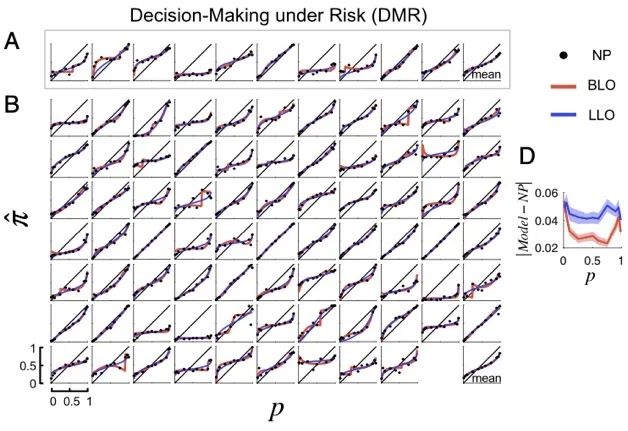
該研究團隊基于被試在DMR*與JRF**兩項認知任務中的行為反應測試了BLO模型的預測表現(模型擬合表現見下圖)。通過多因素模型比較(factorial model comparison)測試,他們發現,減去任何一個因素的部分模型,預測效果都不如完整模型。其次,研究人員將BLO模型與概率失真領域中其他的現存模型進行了比較,結果仍然顯示BLO的預測水平最好。
■ 編者注
*DMR:風險下的經濟決策任務(Decision-Making under Risks tasks):選擇在50%的風險下獲得200美元報償或是一定能獲得的70美元報償;
**JRF:相對頻率的認知判斷任務(Judgement of Relative Frequency tasks)——被試報告屏幕中黑白圓點視覺刺激中黑色與白色的相對比例;
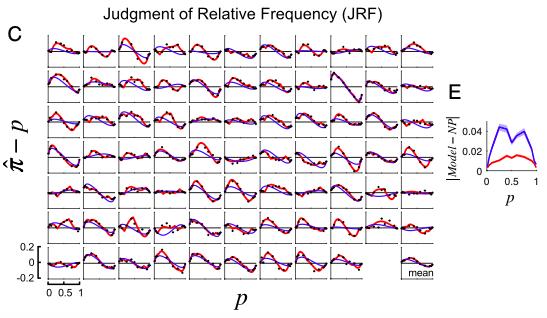
BLO模型的三個假設分別是:
1. 邏輯表征(log-odds representation)
從下圖中我們可以看到,前人研究中出現的概率失真(上列)能夠很好的擬合到邏輯模型中(下列圖片)(注:由上到下對應的是同一組數據的邏輯變換(logistic transformation));
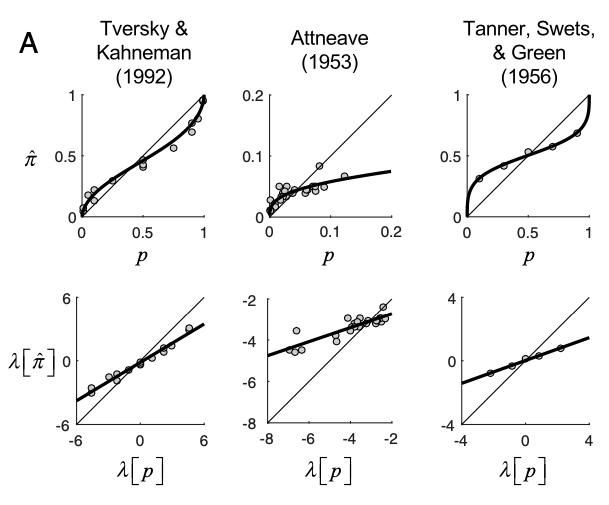
2. 有界性(boundedness):
下圖展示了在概率數值進行了邏輯變換后,從數據中選取兩種大小的區間并將其線性擬合進瑟斯頓裝置(Thurstone device)的方法。我們將進行這種變換后的數據稱為截取后邏輯數據(truncated log-odds);
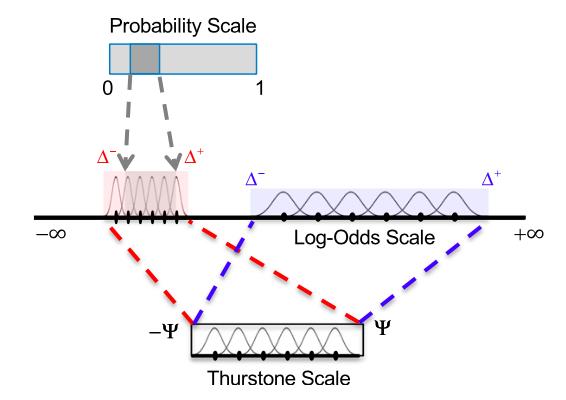
3. 方差補償(variance compensation):
在這里,研究人員利用瑟斯頓尺度(Thurstone scale),從上述變換后的數據中解碼出了被試基于編碼不定性而做出的主觀概率估計。
該研究的重要性在于,現存模型一般只能解釋人們的在某些特定任務決策中出現的概率失真,但BLO模型給出了概率失真背后的一般機制。
doi: 10.1073/pnas.1922401117
“沖動”信號從何而來
Cowley et al., Neuron
每個人都曾做過沖動的決策,這樣的舉動可歸咎于多種認知因素,例如疲勞程度、清醒程度和情感波動等,但這些因素到底是如何影響我們決策的呢?這項研究發現,在獼猴執行視覺辨別任務時,獼猴的視覺皮層V4和前額葉皮層(prefrontal cortex)的活動,會隨著辨別任務的表現,在分鐘級別的時間尺度上共同緩慢地變化。但這樣的變化并不會影響視覺感知本身,而是逐漸發展為一個沖動信號,激發最終的決策行為。
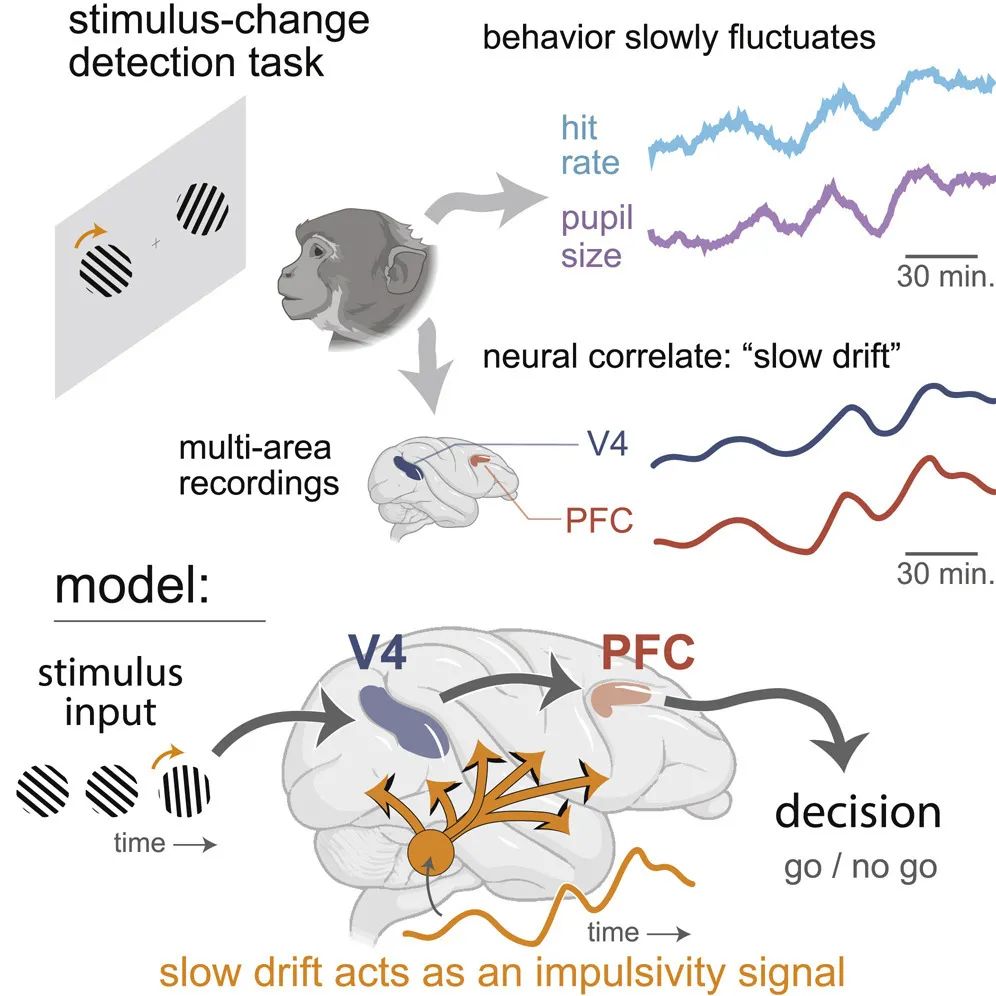
doi: 10.1016/j.neuron.2020.07.021
你的時間感知,會被你的預測控制嗎
Toren et al., Nat. Neurosci.
感知時間和預估未來短期內的事物發展,是人類在日常生活中必不可少的能力。作為大腦重要的時間感知中樞之一,基底神經節(basal ganglia)與多巴胺能神經元有著密集的連接。因為多巴胺能細胞構成了編碼預測錯誤(prediction error)的主要系統,基底神經節有可能在時間感知和預測錯誤之間搭起一座橋梁。在這項研究中,被試需要完成一個時間間隔判斷任務(time-discrimination task)。行為學結果和行為模型數據表明,對未來時間間隔的預測錯誤可以雙向改變時間感知:正向預測錯誤讓被試覺得間隔變長,負向錯誤讓被試覺得間隔變短。不僅如此,被試在做任務時的核磁共振腦成像顯示,紋狀體的活動與預測調控的時間感知有特定的相關性。
doi: 10.1038/s41593-020-0698-3
客觀性錯覺使選民極化
Schwalbe et al., PNAS
民主選舉一向令西方世界,尤其是美國,引以為豪。然而凡事有利有弊、有得有失,政治上的分歧和不信任正在撕裂美國社會。而加劇了這一趨勢的,還有“客觀性錯覺”(objectivity illusion)——我們善于認定“我這邊”的觀點都是客觀公正的,而“他們那邊”的觀點都帶有偏見。
實驗發生在遙遠的2016年,川普和希拉里巔峰對決的前夜。選舉開始的前幾周,川普和希拉里的支持者們已經表現出一種“我們對抗他們”的心理,具體表現是認為和“我”持相同政治立場的人:更加理性、講求證據、目光長遠、少謀私利、難被誤導;而與“我”政治立場相對的人則正好相反。
此外,客觀性錯覺的程度與選民后續對總統選舉辯論的偏見、日后的政治觀點極化(polarization)、觀念的封閉以及對政治對手的反感程度有關。后續的跟進研究發現,兩方選民都對一篇支持對立候選人的杜撰博客表示質疑,并且認為對立政客的支持者是“邪惡的”(evil)。
時光荏苒,白駒過隙,2020年猝不及防地過去了四分之三,而美國又要大選了;哪怕只是中期選舉,這項有關客觀性錯覺研究的發表依然有著超越上一次和這一次選舉的意義,或許能帶給我們一點關于自我和社會的思考和啟發。
doi: 10.1073/pnas.1912301117
系統與網絡
暴飲暴食怎么辦?
藍斑核神經元或許能幫忙
Gong et al., Cell
生活中不難注意到,我們饑餓的時候會覺得饅頭格外香甜,口渴時也會覺得一捧自來水如此讓人心滿意足。我們稱這種由于自身穩態變化而對水和食物產生不同滿足感的現象為適口性 (palatability)。饑餓和口渴雖然驅動著動物獲取不同的目標,但它們都控制著類似的動物攝食行為,從而維持個體生存所需的能量和穩態。然而,我們仍不清楚這些現象的具體機制:為什么饑餓或口渴會改變適口性?這兩種不同的穩態需求是否共用了相同的神經環路,來控制類似的動物行為?
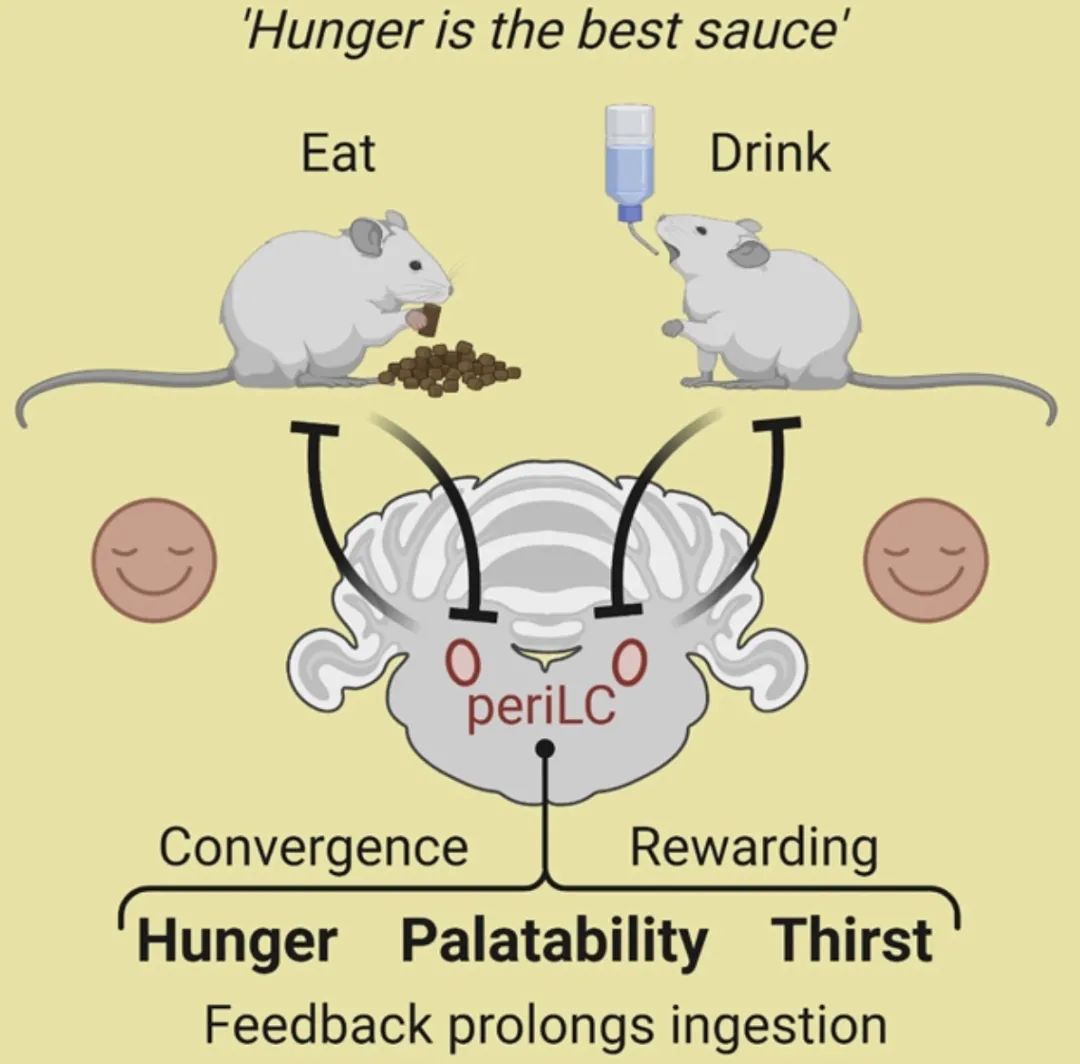
在這篇文章中,研究人員發現位于后腦藍斑核(Locus Coeruleus)的谷氨酸能神經元可以同時調節饑餓和口渴兩種行為,成為進食和飲水這兩條神經環路的調控樞紐。為了進一步研究后腦區神經元在進食和飲水時的活動,他們開發了一種可以穩定觀測自由活動小鼠后腦區鈣離子信號變化的技術。利用這項技術,他們發現藍斑核區的谷氨酸神經元(periLCVGLUT2)能通過傳遞適口性的信息,選擇性地控制自由攝食行為的時長。然而,如果抑制這類神經元,則會導致動物對食物及水的渴望增強,最終導致攝食增加。所以,研究者相信這一條雙負反饋調節通路 (double-negative feedback)可以維持我們對食物和水分的適當攝取。也正因此,periLCVGLUT2通路的紊亂很可能是我們暴飲暴食的重要原因。
doi: 10.1016/j.cell.2020.07.031
眶額葉皮層和紋狀體,
誰在編碼我們的動作選擇?
Yang & Masmanidis, J. Neurophysiol.
眶額葉皮層(orbitofrontal cortex)和背內側紋狀體(dorsomedial striatum)均與動作的選擇有關。不過,迄今為止,尚未有研究系統性地把二者放在同一時間框架下比較其對動作選擇的影響。來自UCLA的研究人員同時記錄了小鼠中這兩個腦區的神經元活動,并訓練小鼠通過向前或向后推動操縱桿來獲取獎勵。作者用向量機解碼兩個腦區中的信號,發現背內側紋狀體能更準確且更迅速地反映動作的選擇。為了排除聲音辨別的影響,作者們指出,當小鼠只有一個可能的動作選擇的時候,或當其沒有做出選擇時,兩個腦區間的區別并不顯著。
盡管這只是一個相關性的研究,但其結果也指向了紋狀體的重要地位:動作選擇的信號甚至可能是先由紋狀體向眶額葉皮層傳播的。
doi: 10.1152/jn.00316.2020
不殘血不會打:
挨餓的斑馬魚為什么更常打勝架?
Nakajo et al., Cell Rep.
如果讓你下注,賭一條挨餓的斑馬魚和吃飽的斑馬魚,誰能打贏對方,你會怎么想?多數人也許會說吃飽的魚更可能打贏,但日本國立理化學研究所(RIKEN)的岡本仁團隊近日表示,在未挨餓的斑馬魚與挨餓6天的斑馬魚之間,后者更有可能打贏對方。
岡本的團隊發現,饑餓能夠增強他們稱為“勝者環路”(winner's pathway)的一條神經環路。這條環路從韁核(habenula)開始,于腳間核(interpeduncular nucleus)結束,傳統上也稱為“韁核腳間束”。腳間核能影響下丘腦,從而調節各種生理過程。饑餓能調高下丘腦食欲素(orexin)的釋放,而食欲素能調控腳間核神經元的AMPA受體電流,使腳間核神經元對上游的韁核輸入更敏感,從而增強“勝者環路”。
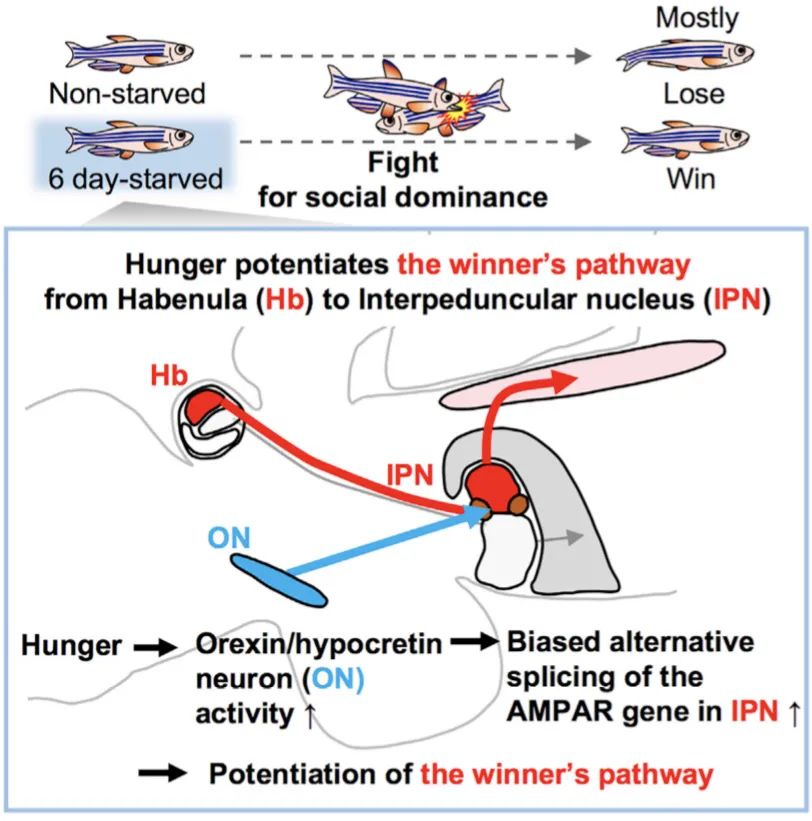
本論文的第一作者中條暖奈認為,這個機制背后的邏輯很簡單:餓了的魚當然更需要食物,而勝者通常可以獲取更多的食物;因此,挨餓的斑馬魚應該更奮力地試著贏得戰斗。
doi: 10.1152/jn.00316.2020
Perspectives | 杏仁核:多維處理器
Gothard, Nat. Rev. Neurosci.
大腦的許多計算都會利用到途經杏仁核的環路,這也意味著杏仁核參與了社會性和非社會性的各種行為。亞利桑那州大學(University of Arizona)的Katalin Gothard教授于近日發表了一篇視角文章,強調了杏仁核作為一個“多維處理器”(multidimensional processor)的重要性。Gothard認為,單個途經杏仁核的神經環路讓社會性行為具有了特定性(specificity),而多個環路在杏仁核中交匯相聚則讓復雜的社會性行為有了很高的可塑性(flexibility)。
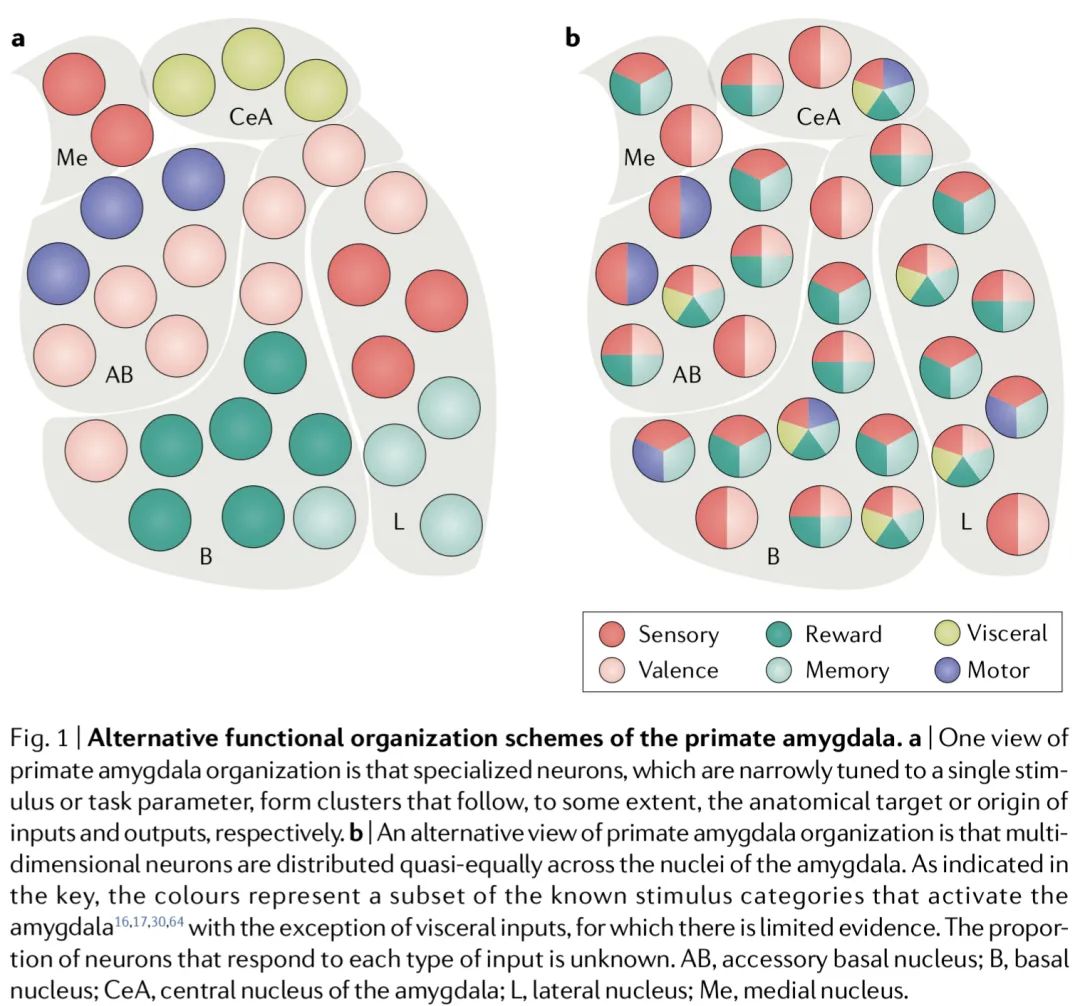
上圖顯示的是學界看待靈長類動物杏仁核的組織結構的兩種方式:a中,杏仁核內對同類刺激產生反應的神經元形成細胞群(clusters),因此各個細胞群都對應了特定的功能(例如左上角,杏仁核內側核團的兩個細胞群都只處理感官信息);b中,杏仁核內的各個細胞群都能處理多維度的信息(例如內側核團中的兩個細胞群能處理獎勵、記憶、感官和價值信息)。越來越多的實驗證據支持b視角。
Gothard在文章末尾表示,對杏仁核組織結構的進一步理解,不能光靠解剖學和生理學研究,還依賴于更多、更詳細的理論研究。這些理論研究既需要考慮杏仁核提供的特定性,也要考慮其允許的可塑性。
doi: 10.1038/s41583-020-0350-y
Review | 線蟲中的非基因遺傳和隔代可塑性
Baugh & Day, eLife
越來越多的研究表明,生物體由于環境因素誘發的表型(phenotype)改變也可以傳遞給后代。尤其跨代可塑性(multigenerational plasticity)的發現,對于傳統的自然選擇理論提出了很大的挑戰。其中,使用線蟲(C. elegans)作為模型的研究帶來了很大的影響:一方面,線蟲展現出了很高的表型可塑性;另一方面,過往的研究都詳細記錄了這種可塑性的分子和細胞機制,然而它們幾乎都不涉及遺傳物質的改變。
這篇綜述總結了使用線蟲作為模型的跨代表型可塑性的研究發現,并指出這些研究對于遺傳和進化的定義往往十分不嚴謹。因此,本綜述的作者為此提出了界定跨代表型可塑性的三項標準:(1)該種群由于環境因素帶來的表型變化可以被傳遞給后代;(2)該跨代表型可塑性可以提升后代的適應性(fitness);(3)能夠提出相應的機制解釋這一現象。作者認為,更加標準地定義跨代表型可塑性,對于該領域的后續研究有重大意義。作者表示,目前許多跨代表型可塑性的實驗發現,都可以被解釋為對非遺傳物質多樣性(nongenetic variation)的選擇而不是適應性跨代表型可塑性的結果(adaptive multigenerational plasticity)。下圖呈現了兩種不同的理論。
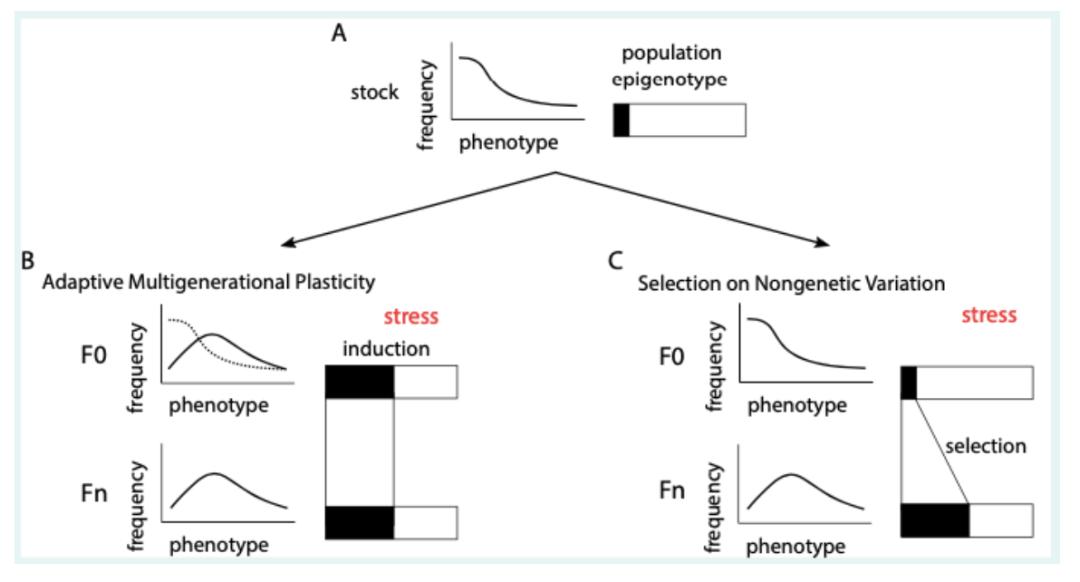
doi: 10.7554/eLife.58498
細胞與分子
搜尋我們腸道里的病毒
Gregory et al., Cell Host Microbe
腸道里并非只有菌群。所謂“腸道微生物群落”(gut microbiome),自然也會包括腸道中的病毒群落(virome)。但至今為止,腸道中的病毒仍未引起較高的關注。這一部分是由于病毒十分難找:與擁有固定標志(例如S16蛋白)的細菌不一樣,病毒不具有固定標志,也因此不能像找尋腸道菌群那樣來搜尋病毒。
Gregory等人另辟蹊徑,利用了機器學習算法,將已知的病毒數據作為訓練樣本,使算法能幫他們搜尋腸道里不同種類的病毒。他們的分析顯示,腸道病毒群落中,占比最大(97.7%)的是針對細菌的噬菌體(phages),其次才是真核細胞病毒和古菌病毒。他們還在真核細胞病毒中發現了一些植物病毒,并表示這很可能只是在腸道里短暫停留的、由食用植物帶入的病毒。
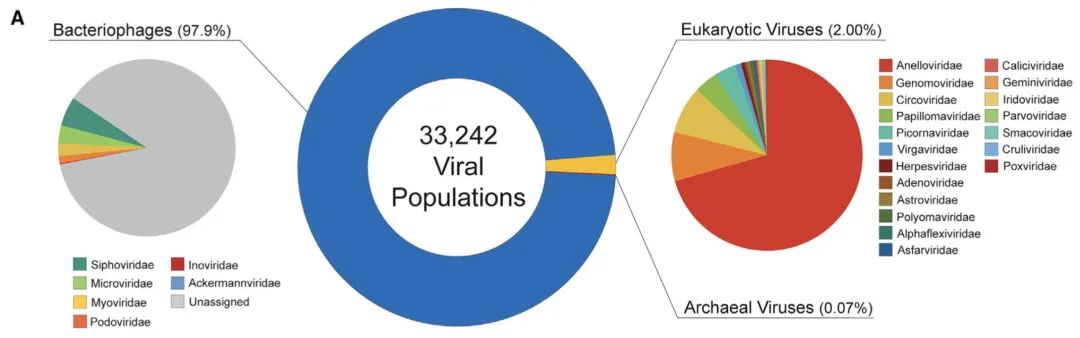
他們還發現,腸道病毒群落中的病毒種類十分因人而異,沒有一種病毒在全部分析個體的腸道中出現。但一個普遍的規則就是,腸道病毒群體的多樣性,從出生開始逐漸增加,直到65歲達到最高點,之后便逐漸下降。Gregory說:“一條黃金準則就是,一個生態系統中的多樣性越高,這個系統就越健康。我們觀察到,更健康的個體(的確)更大概率有更高的病毒群體多樣性,這說明這些病毒也許(對我們)有益。”
doi: 10.1016/j.chom.2020.08.003
突觸周星狀細胞的蛋白局部翻譯或協助學習記憶
Mazaré et al., Cell Rep.
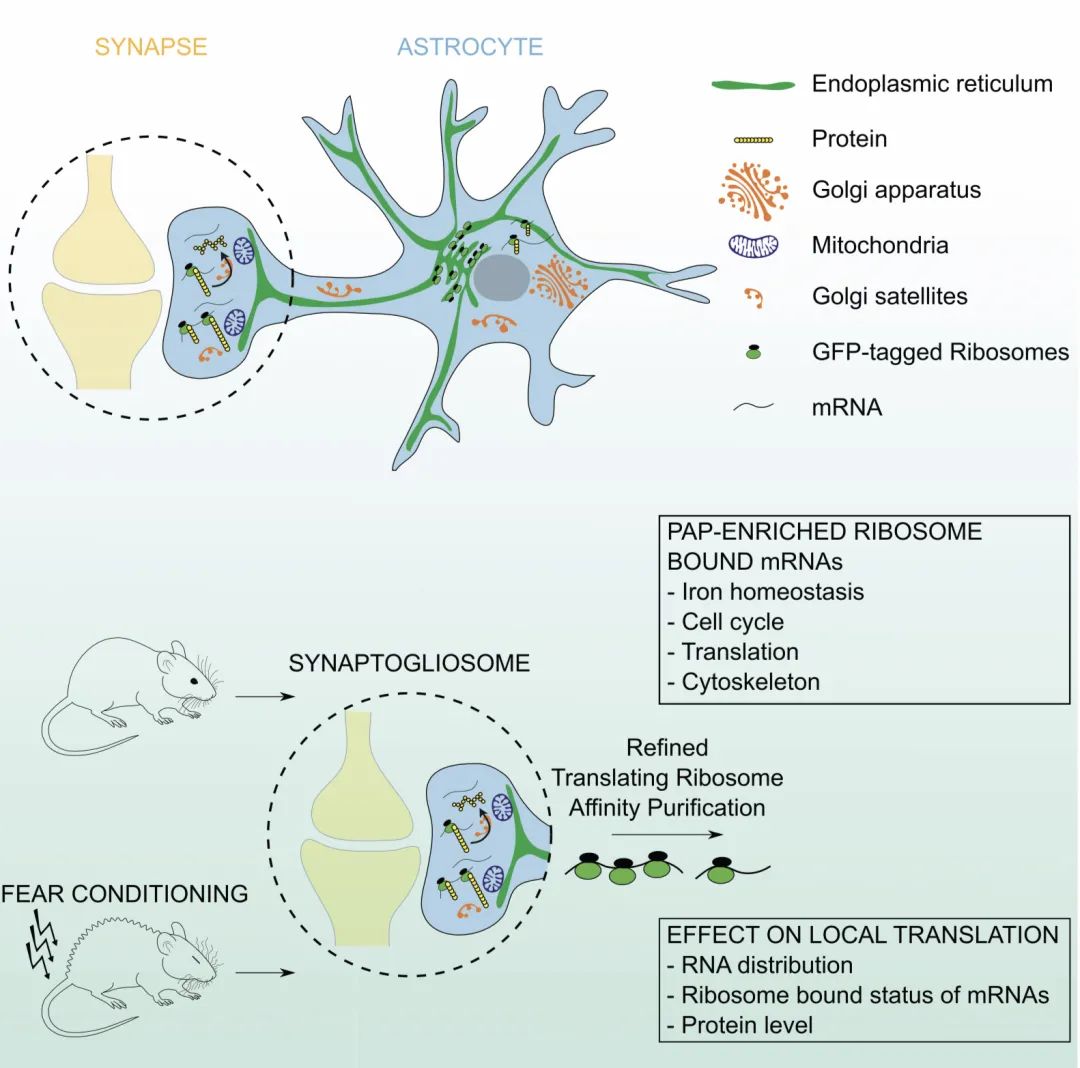
星狀細胞(astrocytes)大量分布于哺乳動物的大腦中并且功能繁多,例如支持腦血管障壁(blood-brain barrier,BBB)的內皮細胞,向神經組織供養,維持胞外離子平衡等等。通常,這些細胞能通過細長而無分支的細胞突起與血管或者神經元接觸,進而發揮作用。近年來,有研究表明在突觸周圍的星狀細胞末端突起 (perisynaptic astrocytic processes,PAPs)可與突觸發生緊密關系,調控突觸的形態及功能。因為細胞內存在著局部蛋白翻譯(local translation)機制,所以細胞能對局部刺激產生快速的反應。那么,能對突觸的變化產生快速應對調節的PAPs,是否也有相應的材料來進行局部蛋白翻譯呢?
在這篇研究中,研究者們利用免疫沉淀技術,確認在PAPs中存在著結合著核糖體的信使核糖核酸 (mRNA),并且相對星狀細胞整體而言,PAPs中的mRNA 分布具有特定的分子極性。他們主要編碼一些參與蛋白質合成,細胞周期調控,離子穩態和細胞骨架的蛋白質。更有趣的是,研究者們發現老鼠在經歷恐懼條件反射(fear conditioning)訓練后,這些大量聚集在PAPs里的轉錄物的分布及翻譯狀態會發生改變。文章作者認為,這些星狀細胞的局部蛋白翻譯過程發生變化很有可能也與學習記憶有關。
doi: 10.1016/j.celrep.2020.108076
疾病與治療
新冠病毒:MassBiologics發現
對抗新冠病毒的單克隆抗體
Ejemel et al., Nat. Commun.
16年前為非典病毒(一種冠狀病毒)開發抗體的MassBiologics,在中國疫情初始就意識到了非典研究的重要性。位于馬薩諸塞州大學(University of Massachusetts)的MassBiologics在年初報告,曾為非典病毒量身定制的抗體,對新冠病毒(SARS-CoV-2)并無顯著作用。但隨著MassBiologics研究人員的繼續努力,王楊(音譯)團隊終于在8月24日報告了一種有效防止新冠病毒與人體細胞ACE2受體結合的單克隆中和抗體(monoclonal neutralising antibodies)——MAb362。
MAb362是一種分泌型IgA(sIgA)抗體。王等人發現,與之前開發的IgG抗體不一樣,MAb362能有效與新冠病毒的刺針蛋白(spike proteins)結合,在其與人體細胞表面的ACE2受體結合前將其攔下。這樣一來,新冠病毒就不能侵入人體細胞,從而失去復制的機會。
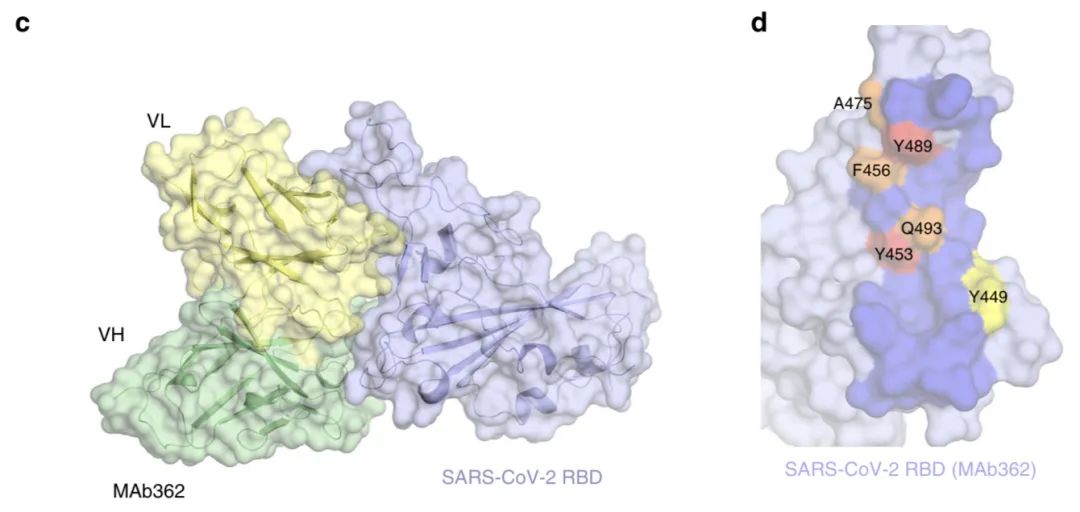
上圖c中,紫色為新冠病毒的受體結合域(receptor binding domain,RBD),黃色為MAb362的輕鏈可變區(variable light,VL),綠色為重鏈可變區(variable heavy,VH)。d顯示的是計算預測的新冠病毒-MAb362結合面,黃色到橙色為抗體上的重點氨基酸。MassBiologics的行政副校監Mark Klempner表示,這種抗體也許能被用于呼吸道粘液上,在新冠病毒入侵的時把好機體的“大門”。
doi: 10.1038/s41467-020-18058-8
新冠病毒:一例新冠病毒孕期傳播病例
Sisman et al., Pediatr. Inf. Dis. J.
九月刊的《兒科傳染性疾病期刊》報導了一例新的新冠病毒孕期傳播病例。在此之前,已陸續有證據表明新冠病毒孕期傳播的存在。這項報導再次強調了孕期防護的重要性。幸運的是,此病例中的母親和孩子都被接收至得克薩斯州大學西南分校醫學中心(University of Texas Southwestern Medical Center),并已被治愈。
doi: 10.1097/INF.0000000000002815
多巴胺可能參與了帕金森病人
對于獎勵相關記憶的優先編碼
Sharp et al., Brain
帕金森病人對于獎勵(reward)的敏感度較低,這可能與多巴胺能神經元的減少以及強化學習(reinforcement learning)能力的損傷有關。然而,越來越多的研究發現,多巴胺能神經元不僅參與了強化學習的過程,還與長期記憶(long-term memory)的鞏固有關。在帕金森病人樣本中,大部分與記憶相關的研究都關注整體記憶容量的多少,而這篇文獻的作者則認為,多巴胺能神經元的活動,可能與某些種類的記憶鞏固相關。因此,研究團隊探究了多巴胺調控以及獎勵對于兩種長期記憶的影響:對于中性物體(neutral objects)的情節記憶(episodic memory),以及對于刺激-價值聯系(stimuli-valence association)的記憶。結果顯示,在帕金森病人中,多巴胺水平的升高與更準確的獎勵記憶有關,但是與整體記憶容量、記憶鞏固的時間無關。
doi:10.1093/brain/awaa182
分析“躲隕石”的走位,
就能明白學習模式
與精神疾病中跨診斷癥狀的聯系?
Wise & Dolan, Nat. Commun.
近年來,跨越傳統疾病診斷邊界的共通癥狀(transdiagnostic symptoms)得到了精神病學領域的關注,而“威脅感知”(threat perception)這一能力的變化,也或許與厭惡性學習(aversive learning)模式的變化相關。為了研究其中的種種聯系,UCL的Toby Wise和Ray Dolan設計了一款需要玩家駕駛飛船穿過一條條隕石帶的游戲,在線收集數據,并找到了一個最優的模型來模擬四百名參與者的行為。這一模型假設人們會根據不同區域上遭遇隕石襲擊的頻率,來確定特定位置會變得更危險還是更安全,并由此參數化了人們學習“威脅性”和“安全性”的速率。他們還分析了玩家的問卷數據,從中分析其焦慮狀態和焦慮特質,以及其自我報告的跨診斷癥狀。
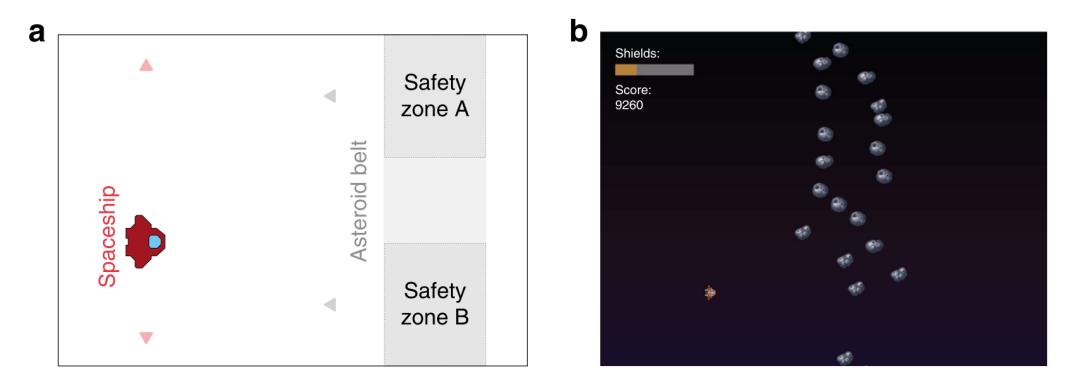
在這一實驗中,具有“強迫性傾向與侵入性思想”這一跨診斷因素者,比其他人更容易用“安全性”來更新他們的預判。與直覺相悖的是,焦慮指數更高的人,竟也展現了類似的學習模式,而非更傾向于學習負面的威脅。
不過,針對分量表的探索性數據分析顯示,認知性焦慮更高,學習“威脅性”的速率的確更高,對安全性的估計也更低。而軀體性焦慮的結果則正好相反。作者們還用偏最小二乘回歸(partial least squares regression)尋找行為與問卷數據中潛在的結構,區分出了兩個獨立的組分:一個同更多的“安全性”的學習、強迫性傾向以及軀體性焦慮相關,而另一個則同更多的“威脅性”學習、抑郁以及社會性焦慮相關。
doi: 10.1038/s41467-020-17977-w
深部腦刺激治療妥瑞氏癥好不好用?
還需看大腦連接性
Johnson et al., Brain
現有理論認為,妥瑞氏癥的病理與皮層-紋狀體-丘腦-皮層環路相關,而嚴重的患者或許可以通過該環路上的深部腦刺激(deep brain stimulation,DBS)來改善癥狀。多國合作的一項回顧性研究,利用白質纖維束成像描述患者腦部的結構連接性,并結合具體刺激區域預測DBS的臨床效果。他們發現,對于接受內側蒼白球(internal segment of globus pallidus,GPi)刺激的患者,與抽動癥狀的改善呈正相關的,是以邊緣系統、前額葉為主的聯合皮層等網絡同受刺激區域的結構連接性;相反,對于接受中央內側丘腦(centromedial thalamus)刺激的患者,呈正相關的是感覺與運動皮層和頂-顳-枕網絡。至于強迫性行為這一共病癥狀,作者們所構建的連接圖譜沒有達到足夠的健壯性,但他們也觀察到了癥狀改善與前額葉、眶額葉皮層以及扣帶皮層(cingulate cortex)的一些聯系。最后,為了找到潛在的、更加精確的DBS靶點,研究人員從這些具有正相關性的腦網絡出發,反推其與受刺激區域的連接性,并注意到,與后腹側蒼白球相比較,前內側蒼白球同這些網絡的連接性更強,且這一區域的刺激能更好地預測抽動癥狀的改善。作者們認為,這些結果或可幫助啟發新的非侵入療法,并改良現有的DBS方案,改變其在隨機對照實驗中表現不佳的僵局。
doi: 10.1093/brain/awaa188
拯救NMDA受體,恢復成年大腦認知
Mielnik et al., Mol. Psychiatry
超過1%的孩子天生患有神經系統發育障礙,對他們的認知能力造成了損傷。近年來,全基因外顯子組測序(whole exome sequencing,WES)技術發現了數百個與這些障礙有關的基因,還新定義了一些綜合征,比如GRIN障礙。GRIN是一組控制N-甲基-D-天冬氨酸型谷氨酸受體(NMDA受體)的基因;7個基因中任一一個出現突變都會被診斷為GRIN障礙。其中,GRIN1、GRIN2A-D和GRIN3A-B上的錯義突變與無義突變導致的腦病有時被診斷為智力殘疾、孤獨癥、癲癇或/和精神分裂。GRIN基因突變主要通過降低NMDA受體的功能致病。
此前的研究表明,NMDA受體在神經系統中舉足輕重:興奮性和抑制性突觸的正常發育,丘腦及大腦皮層中感官環路的正常連結都需要NMDA受體的參與;敲除NMDA受體的小鼠在適應新環境、處理聲音驚嚇(acoustic startle)、社交互動和焦慮方面都會受損。因此很容易推測,如此重要的NMDA受體在成年大腦中應當相對穩定,比較難以干預。這是生物體對重要部件的保護措施,也是治療重要部件錯誤導致的疾病的一大障礙。
好消息是,這項新研究表明,成年大腦中的NMDA受體并非不可拯救。研究人員建立了一個先天GRIN1等位基因失效的小鼠模型,利用可以三苯氧胺誘導(tamoxifen-inducible)的Cre重組酶在成年小鼠的大腦中短暫地恢復了NMDA受體,有效且相對長時間地緩解了小鼠的認知功能,包括對新環境的適應、聲音驚嚇的處理、社交互動和焦慮。最令人驚訝的是,研究結果表明,認知損傷(智力殘疾)——一個廣泛存在于GRIN障礙中但現存藥理治療束手無策的癥狀——是可以在成年大腦中修復的。而對成年大腦進行基因治療更是一個極具潛力且振奮人心的臨床方法,它意味著從病發到治療之間的延遲或許可以被克服,我們能夠幫助成年人重獲穩定的正常功能。
不過,路漫漫其修遠兮,小鼠實驗與臨床應用還有很長的距離。若論這篇文獻能帶來什么感慨,怕是再一次驚嘆于大腦的可塑性吧。
doi: 10.1038/s41380-020-00859-4
干細胞外排體與孤獨癥
Perets et al., Mol. Autism
SHANK3基因的部分或完全缺失被認為是Phelan-McDermid綜合征(又稱“22q13.3缺失癥候群”)的主要病因。這種綜合征的患者中,有75%被診斷為孤獨癥。近年來,越來越多的研究人員開始關注孤獨癥的干細胞療法,其中尤以間充質干細胞(mesenchymal stem cells,MSC)為熱門候選。
本文團隊此前的研究已經發現,腦室間MSC注射(interventrical administration of MSCs)能夠緩解BTBR孤獨癥模型小鼠(一種常用的孤獨癥模型動物)的核心癥狀,包括社交和母性行為的顯著改善、重復性行為的減少和認知僵化(rigidity)程度的降低;這種療法的效果至少能維持6個月之久。鑒于MSC在移植組織內大概率只能存活數周,研究人員推測MSC注射的有效性應該來自其持久有效的旁分泌作用(paracrine secretion)。后續的研究支持了這一推測,并且指出,MSC依靠分泌外排體(exosome)達到持久的療效。外排體是一種納米級的脂質小囊泡,負責攜帶蛋白質、RNA和小分子RNA(miRNA),也部分細胞間交流有關。
另外,用人類MSC外排體對BTBR小鼠進行鼻腔給藥能夠顯著改善孤獨癥核心癥狀。有趣的是,這些外排體會遷移到鼠類模型中特定的神經病理學部位,包括了中風、帕金森病、阿爾茲海默病、脊髓損傷和孤獨癥模型。
然而,BTBR模型是一種特發性孤獨癥模型,致病基因未知。為了探究MSC外排體對有單一致病基因突變的孤獨癥模型的療效,本研究選用了Shank3基因敲除小鼠,并對它們的社會和認知能力進行評估。Shank3是一種存在于興奮神經元突觸后致密物質(postsynaptic density)中的重要支架蛋白質 (scaffold protein),攜帶Shank3基因失活變異的小鼠展示出穩健的孤獨癥行為表型。進行MSC外排體鼻腔給藥后,這些Shank3敲除小鼠在社交互動、理毛行為和超聲發聲(ultrasonic vocalisation,小鼠的交流方式)方面都有了顯著的進步,在BTBR模型給藥后出現變化的炎性RNA標記(TNF,IL-1和IBA-1等炎癥因子的RNA)在Shank3模型中沒有變化。
對孤獨癥癥狀的神經學解釋中,有一種關注的是大腦內興奮-抑制平衡的變化——孤獨癥患者的GABAA受體有下調。此研究中,小鼠模型里也發現了GABA Ra1 RNA微小但顯著的增加。
當然,最重要的發現還是孤獨癥核心癥狀的緩解。相比對照組,接受MSC外排體鼻腔給藥的小鼠表現出更接近野生模型(正常小鼠)的行為模式。這項研究表明,外排體可以被列為緩解Phelan-McDermid綜合征患者孤獨癥癥狀的臨床候選。
相比前面講過的重組酶拯救NMDA受體,恢復成年大腦認知能力的提議(見“拯救NMDA受體,恢復成年大腦認知”),這項提議聽上去要少受不少罪呢。
doi: 10.1186/s13229-020-00366-x
Pre-proof | 母體免疫激活與孤獨癥
Ren et al., Brain Behav. Immun.
除了社交障礙和重復性行為,許多孤獨癥患者的感覺處理(sensory processing)也有一定的缺陷;視力受損及其導致的行動異常是其中一種。然而,孤獨癥是一種異質性極高的障礙,癥狀的表現更是五花八門不盡相同。視力方面,孤獨癥患者對不同空間頻率和對比度的光柵刺激可以表現出正常、過高或過低的反應(也就是說啥情況都有)。因此,對于孤獨癥癥狀的研究需要謹慎篩選合適的模型。
孤獨癥的病因至今尚不明確,一般認為許多不同因素都可能致病。其中,胚胎期母體免疫激活常被報告,業內達成了一定程度的共識。這項研究旨在探索母體免疫激活和后代視力之間的關系。通過給懷孕的小鼠腹腔注射聚肌胞苷酸(polyinosinic-polycytidylic acid,簡稱polyI:C),小鼠會產生母體免疫激活,它們的雄性后代在4-6周大或者3個月大時進行了視覺運動反應測試。同時,研究人員還對年輕的成年個體(4-6周大)外側膝狀體的背側核進行了切片觀察。
結果表明,由polyI:C導致的母體免疫激活會降低(雄性)后代的視力,并且阻礙視網膜神經纖維投射的修剪(retinogeniculate axon elimination)。研究人員認為,視力不僅和視網膜光感受器的排列有關,視覺信息從視網膜到視覺丘腦的傳遞質量也能影響視力。母體免疫激活阻礙了投射的精煉(refinement),使得突觸強度減弱,中繼(relay)信息的效率降低,由此影響后代的視力。
值得注意的是,研究人員在母體免疫激活組和對照組的小鼠中并沒有發現社交能力的差別。因此,該實驗僅能支持母體激活免疫可以阻礙神經投射正常發育降低后代視力,無法為其與孤獨癥的關系提供直接證據。
另外,研究人員似乎沒有明確討論為什么僅選用了雄性后代,又將結論擴展至“后代”。鑒于這還是pre-proof,或許正式發表時能有更清晰的闡述。
doi: 10.1016/j.bbi.2020.08.017
熊貓新聞
熊貓美香產下第四胎
身在華盛頓特區的國家動物園(National Zoo),22歲的美香(下圖,攝于8月23日)于8月21日又產下一只熊貓崽。在這個年紀再產下后代是少有的事。美香之前的三個孩子(泰山、寶寶和貝貝)都已被護送回中國。目睹美香產下第四胎的動物園發言人Pamela Baker-Masson女士說:“我們需要這種單純的喜悅!”

—
中國新聞網
編者:阿莫東森、狗尾巴花、山雞、航跡云、圖圖、小鹽、肖本
排版:小葵花
封面:紀善生
原標題:《用抗體治療新冠病毒有戲嗎?;暴飲暴食?藍斑核神經元或能幫忙;你的預測,如何影響你的時間感知? | Paper Alert #8》
本文為澎湃號作者或機構在澎湃新聞上傳并發布,僅代表該作者或機構觀點,不代表澎湃新聞的觀點或立場,澎湃新聞僅提供信息發布平臺。申請澎湃號請用電腦訪問http://renzheng.thepaper.cn。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




