- +1
全球首例治療COVID-19臨床實驗研究公布,抗艾滋病藥物克力芝收效甚微
編輯小文 世界頂尖科學家論壇

這是新冠病毒疫情暴發(fā)以來,世界頂級醫(yī)學雜志首次發(fā)表治療COVID-19的臨床試驗結果,也是在包括SARS在內(nèi)的近20年新發(fā)傳染病疫情期間發(fā)表的屈指可數(shù)的藥物臨床試驗結果。同期配發(fā)的NEJM社論稱贊該臨床試驗為英勇之舉。
該項研究的通訊作者為中日友好醫(yī)院副院長、呼吸與危重癥醫(yī)學科主任曹彬,武漢市金銀潭醫(yī)院院長張定宇,中國工程院副院長、中國醫(yī)學科學院北京協(xié)和醫(yī)院院長、國家呼吸疾病臨床醫(yī)學研究中心主任王辰。另一項名為瑞德西韋的治療COVID-19的潛在藥物的臨床研究也由曹彬、王辰領銜。
洛匹那韋 / 利托那韋商品名克力芝,屬于 HIV - 蛋白酶抑制劑。從1月23日中國國家衛(wèi)健委辦法的《新型冠狀病毒感染的肺炎診療方案》(試行第三版),就將克力芝納入國家推薦的藥物中。該藥在新冠肺炎治療上的效果以及安全性方面一直頗具爭議。

該研究在199例確診重癥患者中展開,是一項遵守隨機、對照、開放標簽的嚴格臨床科學試驗。其中,99例被隨機分配至洛匹那韋-利托那韋組,100例被隨機分配至常規(guī)治療組。分別接受常規(guī)治療聯(lián)合14日的每日兩次洛匹那韋-利托那韋(分別為400mg和100mg)治療或者單獨常規(guī)治療。
主要判斷的依據(jù)是至臨床狀況改善的時間,其定義為從隨機分組至7分等級量表評分改善2分或者出院(以先發(fā)生的一項為準)的時間,以先發(fā)生的一項為準。
研究團隊介紹:臨床狀況改善終點的判定曾被用于流感研究中,也是WHO研發(fā)藍圖(R&D Blueprint)專家組推薦的標準。等級量表在之前已被用作重癥流感住院患者臨床試驗的終點。
7分等級量表包括以下等級:
1. 未住院,且可繼續(xù)從事日常活動;
2. 未住院,但無法繼續(xù)從事日常活動;
3. 住院治療,不需要吸氧;
4. 住院治療,需要吸氧;
5. 住院治療,需要經(jīng)鼻高流量氧療、無創(chuàng)機械通氣或這兩者;
6. 住院治療,需要ECMO、有創(chuàng)機械通氣或這兩者均需要;
7. 死亡。
其他臨床結局包括在第7日和第14日時采用7分等級量表評估的臨床狀況、28日死亡率、機械通氣持續(xù)時間、生存者的住院時長以及從治療開始至死亡的時間(天數(shù))。
病毒學指標包括隨時間推移,檢出病毒RNA的患者比例以及病毒RNA滴度曲線下面積(AUC)測定值。
安全性結局包括治療期間發(fā)生的不良事件、嚴重不良事件和提前停止治療。不良事件根據(jù)美國國立癌癥研究所《不良事件通用術語標準》(National Cancer Institute Common Terminology Criteria forAdverse Events)4.0版進行分級。
很遺憾的是,研究顯示,洛匹那韋 / 利托那韋收益甚微。
臨床狀況改善的時間方面,洛匹那韋-利托那韋治療與常規(guī)治療無差異。
洛匹那韋-利托那韋組和常規(guī)治療組的28日死亡率相似(19.2%vs.25.0%;差異,-5.8個百分點;95% CI,-17.3~5.7)。
兩組在各時間點可檢出病毒RNA的患者百分比相似。
在改良意向治療分析中,與常規(guī)治療相比,洛匹那韋-利托那韋治療使至臨床狀況改善的中位時間提前了1天(風險比,1.39;95% CI,1.00~1.91)。
洛匹那韋-利托那韋組的胃腸道不良事件發(fā)生率較高,但常規(guī)治療組的嚴重不良事件發(fā)生率較高。13例患者(13.8%)因不良事件提前停止洛匹那韋-利托那韋治療。
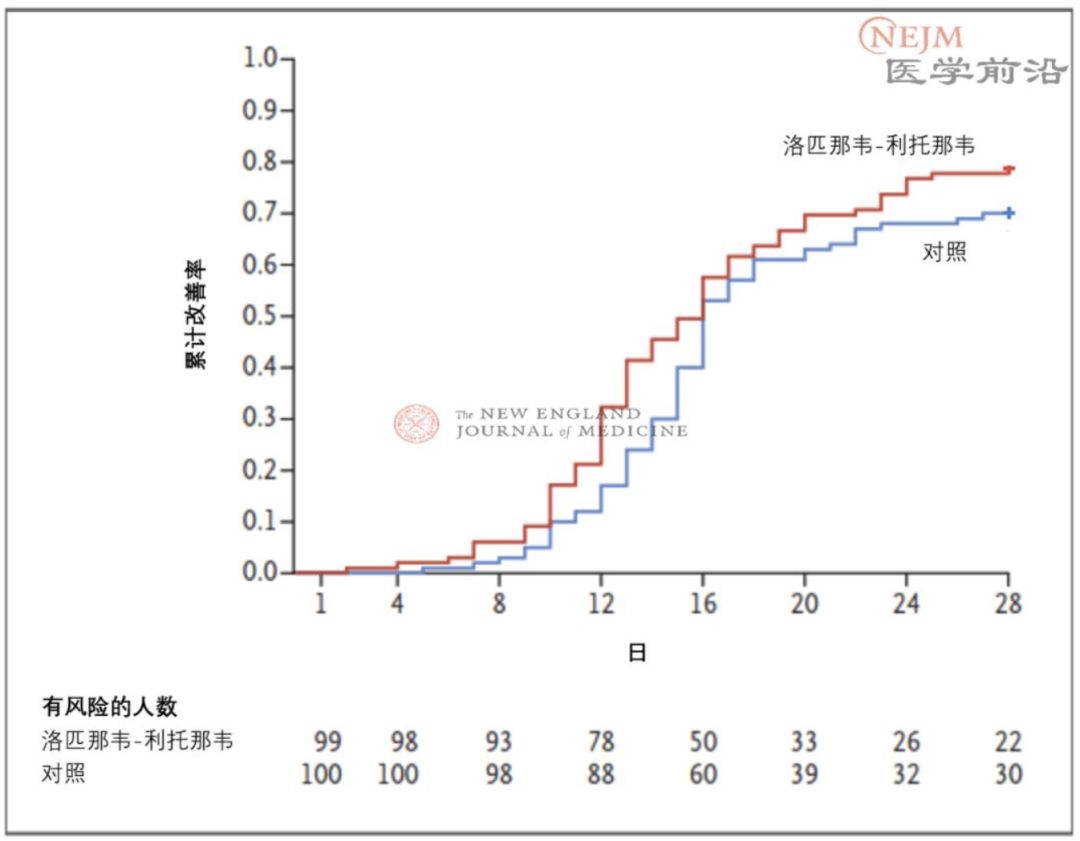
研究團隊也指出了本試驗有幾項局限性。其中尤其重要的是本試驗未采用盲法,因此知曉分組情況可能影響了臨床決策,進而可能影響了7分等級量表的使用。研究團隊指出將繼續(xù)隨訪這些患者,評估其遠期預后。兩組患者的基線特征基本平衡,但洛匹那韋-利托那韋組的咽喉部病毒載量略高,因此該組的病毒復制可能較多。
研究團隊指出,雖然洛匹那韋-利托那韋未能顯著加速臨床狀況的改善,未能降低死亡率,也未能減少咽喉部檢出的病毒RNA。但這些早期數(shù)據(jù)將為未來開展研究評估該方案和其他藥物對新冠病毒感染的療效提供指導。SARS治療中曾將洛匹那韋-利托那韋與其他抗病毒藥聯(lián)用,目前也正在MERS-CoV中研究聯(lián)合用藥,而在COVID-19治療中將洛匹那韋-利托那韋與其他抗病毒藥聯(lián)用可否增強抗病毒效果,改善患者臨床結局仍有待確定。

為什么洛匹那韋-利托那韋沒有顯示更有效,可能有兩個主要原因:
1、作者選擇了一個特別具有挑戰(zhàn)性的人群。
由于參與研究的患者都是危重病患,已經(jīng)有相當大的組織損傷(對照組肺功能受損,死亡率為25%)。即使是高活性的抗菌藥物對晚期細菌性肺炎的療效也有限。
2、洛匹那韋并不是治療SARS-CoV-2的針對性藥物。與使用洛匹那韋-利托那韋治療的患者的血清水平相比,抑制病毒復制所需的藥物濃度相對較高。目前對抑制SARS-CoV-2復制說需的藥物濃度知之甚少。
編輯評論同時提出:試驗是在病毒被確診后幾天內(nèi)開始的,而且感染測試的開發(fā)和部署非常迅速,這意味著測試特征尚未完全確定。值得注意的是,35%的通過鼻咽拭子檢測出SARS-CoV-2陽性的患者在第一天通過口咽拭子檢測時呈陰性。這是由于評估地點、患病時間、測試特征的不同,還是僅僅是疾病的自然演變?此外,42%的患者在第28天病毒載量呈陽性,但當時的定量數(shù)據(jù)顯示,病毒載量很低,可能接近檢測閾值。由于該檢測檢測到核酸,陽性結果并不一定表明感染病毒的產(chǎn)生。這些數(shù)據(jù)表明,評估從嚴重疾病中恢復后的傳播能力將是幫助控制傳播的優(yōu)先事項。
評論指出,盡管洛匹那韋-利托那韋對Covid-19患者的療效似乎不高,但這項研究有許多重要的收獲。調(diào)查人員適當?shù)卮_定了速度的優(yōu)先順序,設計了一個能夠迅速得出答案的試驗。很明顯,快速啟動的高質(zhì)量隨機臨床試驗在流行病情況下也是可能的。隨著危險的冠狀病毒爆發(fā)的繼續(xù),這些試驗的結果,無論是令人信服的陽性結果還是令人信服的陰性結果,都將成為臨床治療的中心。
論文鏈接:
https://www.nejm.org/doi/full/10.1056/NEJMoa2001282?query=featured_home
評論鏈接:
https://www.nejm.org/doi/full/10.1056/NEJMe2005477
本文為澎湃號作者或機構在澎湃新聞上傳并發(fā)布,僅代表該作者或機構觀點,不代表澎湃新聞的觀點或立場,澎湃新聞僅提供信息發(fā)布平臺。申請澎湃號請用電腦訪問http://renzheng.thepaper.cn。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯(lián)網(wǎng)新聞信息服務許可證:31120170006
增值電信業(yè)務經(jīng)營許可證:滬B2-2017116
? 2014-2025 上海東方報業(yè)有限公司




