- +1
醫療科技評論 | iCares: 用于慢性傷口滲出液管理和分析的微流控可穿戴設備
在醫學領域,慢性傷口(如糖尿病足、靜脈性潰瘍等)一直是最令人頭疼的“沉默負擔”。它們恢復緩慢、感染率高、治療周期長,嚴重影響患者生活質量,也造成巨大的醫療負擔,造成了相當大的經濟負擔,并深刻影響了患者的生活質量。準確預測傷口愈合狀態對于做出明智的決策和根據患者特定需求及時進行個性化干預至關重要,從而有可能縮短恢復時間并改善整體結果。
4月23日,加州理工學院的研究者們在《科學轉化醫學》發表研究文章,他們設計了一種可穿戴設備 iCares,用于優化緩慢釋放的傷口液的收集并感應活性氧和氮物質、pH 值和溫度。在糖尿病小鼠中,傳感器檢測到皮膚傷口感染期間這些因素的變化,并通過抗生素治療使得它們消退。在 20 名慢性傷口人類患者的隊列中,iCares 多參數傳感器測量與機器學習算法配對,以對傷口的嚴重程度和愈合的可能性進行分類。這種原位傷口滲出液分析的進一步發展可以提供對傷口狀態的客觀評估,為慢性傷口的治療決策提供信息。——Molly Ogle(編輯總結)
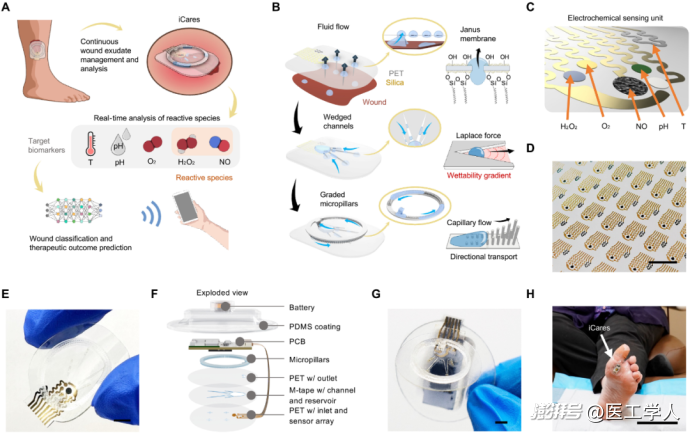
圖1 iCares,一種用于傷口滲出液管理、反應性物種分析和個性化傷口評估的無線智能繃帶
1 研究框架:從采樣到AI決策的閉環系統
這項研究的最大亮點在于為解決慢性傷口滲出液采集難、分析難、連續監測難的挑戰,研究團隊提出的集“微流控采集 + 柔性傳感 + 無線通信”于一體的iCares智能繃帶系統,其結構設計可劃分為以下幾個核心模塊:
圖1展示了iCares的完整構成,從外形上看,它是一個貼附于傷口表面的智能創口貼。其核心特征包括:
1. 柔性多參數傳感器陣列(圖1C):可檢測NO、H?O?、O?、pH、溫度。
2. 三層微流控結構(圖1B):
* Janus膜(超疏水/超親水)促進單向液體流動;
* 楔形通道加速液體吸入;
* 漸變微柱用于流體更新。
3. 層疊式封裝結構(圖1F):
* 從底到頂依次為PET基底、電極層、微流控通道層、感測模塊、無線通信PCB、電池、PDMS保護層。
4. 無線通信模塊(圖1G):通過藍牙實時傳輸生化數據至移動終端。
5. 臨床適配能力:兼容Tegaderm等商用醫用貼膜,可無創貼附于人體傷口(圖1H)。
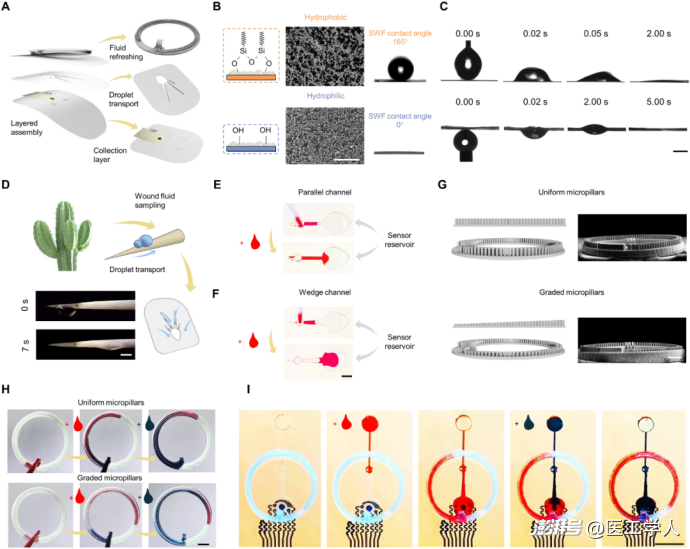
圖2 用于高效傷口滲出液管理的 triad 微流體模塊的設計和表征
圖2集中展示了iCares中最關鍵的“微流控液體管理系統”,其結構獨特之處在于無需泵、電源或外部操作,即可實現:
1. 高效采集(Janus膜)
圖2B/C中展示的Janus膜由涂覆納米二氧化硅的PET制成,一面超疏水,一面超親水,利用拉普拉斯壓力差形成單向流體通路;
膜孔徑為100 μm,間距100 μm,支持均勻、快速液體通過。
2. 導液傳輸(楔形通道)
圖2E/F中對比了楔形與普通通道,借鑒仙人掌刺水收集原理,設計了6°夾角的楔形結構,大大提升了液體傳輸速率;
數值模擬驗證了此設計的液體導向優勢。
3. 液體更新(漸變微柱)
圖2G/H展示了漸變高度的三維微柱陣列,利用毛細力差異實現液體自動“刷新”;
采用紅藍染料實驗驗證:與均勻微柱相比,漸變結構幾乎可消除液體交叉混合,保證時間分辨率。
4. 整體自動操作(圖2I)
在連續液體滴加實驗中,前一滴液體(紅色)會被“推出”感應區,后一滴液體(藍色)自動進入,整個過程無需主動控制。
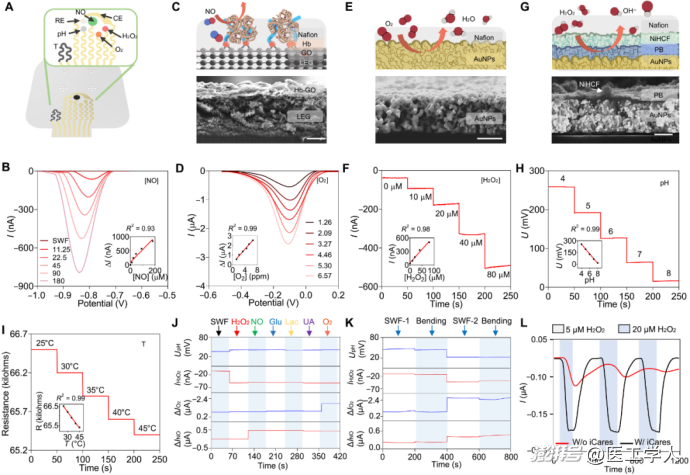
圖3 柔性多參數電化學傳感器 高靈敏,多指標,抗干擾
圖3 聚焦于傳感器陣列的材料、結構與電化學性能優化,核心內容如下:
1. NO傳感器(圖3B/C)
* 使用激光刻蝕石墨烯(LEG)與石墨烯氧化物(GO)構建電極;
* 血紅蛋白(Hb)作為識別分子,能夠在?0.8 V下將NO還原為N?O,從而實現高選擇性檢測;
* 在模擬傷口液中對NO濃度(0.5–45 μM)呈線性響應,抗干擾能力極強。
2. O?傳感器(圖3D/E)
* 采用噴墨打印金納米顆粒(AuNP)電極,在?0.15 V下檢測氧還原;
* 響應范圍1.26–6.57 ppm,靈敏度優良。
3. H?O?傳感器(圖3F/G)
以普魯士藍(PB)/六氰鐵鎳(NiHCF)雙層修飾電極,提高中性pH環境下穩定性;
檢測限達0.25 μM,靈敏度5.91 nA/μM。
4. pH與溫度傳感器(圖3H/I)
* pH傳感器基于電聚合苯胺(PANI),可在pH 6–8范圍內穩定工作;
* 溫度傳感器基于碳墨阻性變化,支持傳感器校準。
* 系統穩定性與多參數協同(圖3J–L)
* 設備在機械變形(如50次彎折)后依然保持響應穩定;
* 多參數聯合監測顯示良好互補性和無明顯交叉干擾;
* 微流控系統的存在大幅提升了動態濃度變化響應的準確性與穩定性(圖3L)。
通過上述集成設計,iCares不僅僅是一塊“高科技繃帶”,更是一個可持續運行的“現場實驗室”,將復雜的生理信號轉化為可被AI解析的數據,為傷口管理提供“感知+決策”新范式。
2 臨床意義:讓慢性傷口管理從“經驗”邁入“數據時代”
1. 實時監測,早期預警
在小鼠模型中,iCares能在感染臨床癥狀出現前通過H?O?等信號檢測出傷口異常,實現早干預、早治療。
2. 人體實驗驗證,準確預測
在20位慢性傷口患者的臨床應用中,AI模型對愈合時間預測的準確率高達94%。對于慢性傷口的個性化治療與資源優化配置具有重要價值。
3. 適用于資源受限地區
傳統傷口管理需頻繁前往專科醫院,iCares則有望實現居家穿戴、自主監測、遠程干預,尤其適用于老齡患者和發展中國家的基層醫療場景。
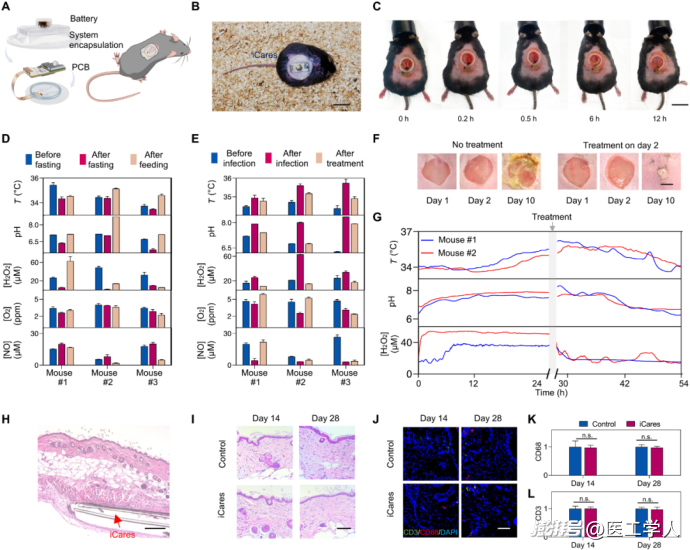
圖4 使用糖尿病小鼠模型對 iCares 進行體內評估
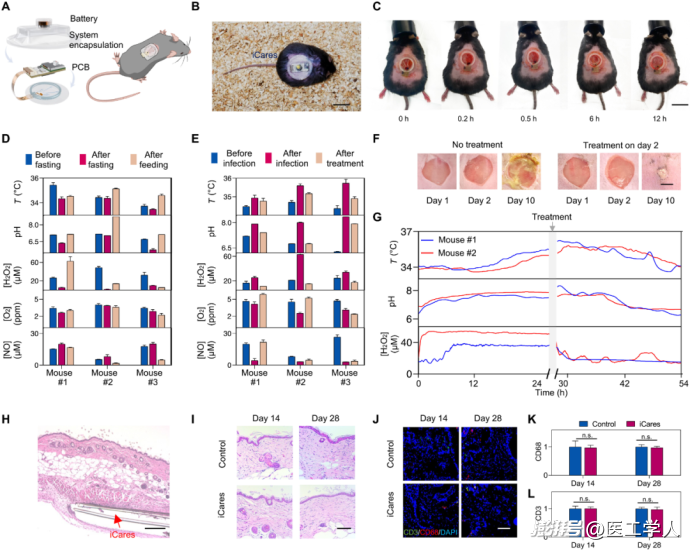
圖5 人工智能驅動的 iCares 在慢性傷口患者中的體內評估
3 科學洞察:從生理過程到治療反饋的“透明窗口”
iCares的關鍵優勢在于將傷口“不可見”的內在變化變為“可見”的數字信號——
NO反映血流重建與免疫調節;
H?O?是感染與氧化應激的重要信號;
O?含量關系到局部供血與組織代謝。
當這些指標被連續監測并以AI模型處理后,就像為傷口“裝上了傳感器+大腦”,具備了感知-分析-響應的智能能力。
盡管該研究已經提供了關于傷口滲出物采樣、監測和分析的有希望的初步數據。但是,也存在幾個限制。第一,盡管 iCares 系統的設計是柔性的,但其固定的形狀限制了它適應不同深度、不規則輪廓或愈合過程中動態變化的傷口的能力。第二,可以使用激光切割、噴墨打印和 3D 打印大規模制造 iCare 組件;裝配過程需要精確對中和手動作。這種復雜性可能會給大規模生產和一致性帶來挑戰,從而可能影響可重復性。第三,iCares 系統主要是為監測而設計的,不包括集成治療模塊。
最后,該研究缺乏足夠的臨床驗證,因為傷口狀態與傷口滲出液中各種生物標志物之間的相關性仍未完全確定。解決這一差距需要全面的臨床試驗來驗證我們的發現并提高這些生物標志物在不同傷口條件下的預測準確性。通過對不同的患者群體進行廣泛的臨床試驗以驗證系統的有效性和可靠性,研究者在文章中寫道:預計未來的研究將大大加強慢性傷口管理,提供更精確的數據驅動方法來改善患者護理和治療結果,同時減輕醫療保健提供者的負擔。
Canran Wang et al., A microfluidic wearable device for wound exudate management and analysis in human chronic wounds.Sci. Transl. Med.17,eadt0882(2025).DOI:10.1126/scitranslmed.adt0882
END
撰文 | 羅虎
審核 | 醫工學人理事會

本文為澎湃號作者或機構在澎湃新聞上傳并發布,僅代表該作者或機構觀點,不代表澎湃新聞的觀點或立場,澎湃新聞僅提供信息發布平臺。申請澎湃號請用電腦訪問http://renzheng.thepaper.cn。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




