- +1
干細胞美容亂象多,這個行業標準回答如何獲得標準干細胞制劑
市面上宣傳的“干細胞美容”靠譜嗎?
“在我國,干細胞制劑從未被批準應用于整形美容,如果市場上宣傳從脂肪中提取干細胞、再進行臉部注射美容的做法,那是違規的,也沒有任何科學研究的基礎,當前提取的干細胞仍然在臨床研究階段。”中國整形美容協會副會長、上海交通大學醫學院附屬第九人民醫院副院長、整復外科主任李青峰表示,只有獲得標準的干細胞制劑,才有可能知道可以拿它來治療什么病。
如何獲得符合標準的干細胞制劑?
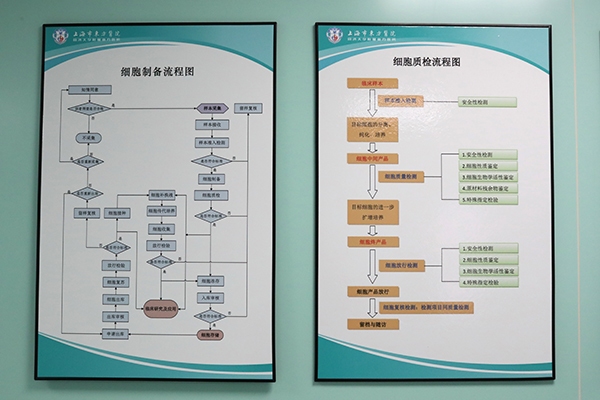
1月30日下午發布的《干細胞制劑制備與質檢行業標準(試行)》為獲得干細胞制劑提供了規范。該行業標準由中國整形美容協會干細胞研究與應用分會會長、同濟大學附屬東方醫院院長劉中民教授研究團隊,在征求近30名干細胞相關領域權威專家的基礎上,歷時兩年多整理形成。
劉中民說,《干細胞制劑制備與質檢行業標準(試行)》可以說是目前國內覆蓋干細胞種類廣、覆蓋流程全、適用范圍寬的聚焦干細胞制劑制備和質檢的行業標準,但值得一提的是,這一行業標準并非干細胞治療臨床應用的標準,僅僅只是針對干細胞制劑生產過程中的質控標準,“遵循這一標準去生產干細胞制劑,其安全性可以得到保證。”

規范“如何獲得標準的干細胞制劑”
“干細胞猶如‘種子細胞’,是一類具有自我更新并可定向分化為特定功能細胞的原始細胞群體,理論上具有全能性的干細胞在一定條件下可以分化為任何一種組織細胞,實現人體組織再生。”劉中民表示。
劉中民說,當前,干細胞治療人類疾病已經成為彌補傳統治療不可或缺的有效手段,隨著干細胞在治療重大慢性疾病、嚴重創傷修復方面的地位和價值日益凸顯,干細胞正在徹底顛覆傳統醫學,引領生物醫藥領域新一輪的科技革命和產業變革。
上海也在干細胞研究方面作出了一系列努力。
2014年12月,張江重大項目——干細胞轉化醫學產業基地項目獲批,項目總經費投入2.55億元。2018年11月11日,張江項目二期又獲批,項目總投入經費2.5676億元,其中資助專項經費1.25億元。
而在2018年10月26日,東方醫院代表同濟大學牽頭,聯合復旦、交大、海軍軍醫大學、中科院上海生科院申報的“干細胞與轉化”被納入上海市IV類高峰學科,建設經費5000萬。其中,東方醫院重點聚焦干細胞治療心衰、骨關節炎、糖尿病等重大疾病的臨床轉化。
然而,劉中民進一步指出,在干細胞基礎研究和轉化應用快速發展的同時,干細胞研究單位難以獲取來源清晰、質量可控的干細胞制劑,由此導致當前干細胞臨床研究項目數量不足。
“從2015年國家出臺《干細胞臨床研究管理辦法(試行)》以來3年多,對于干細胞臨床研究實施項目備案,102家干細胞研究單位在國家衛健委和藥監局完成了干細胞臨床研究機構備案,12家部隊醫院在中國人民解放軍總后勤部完成了干細胞臨床研究機構備案,完成備案的項目目前僅有35項。” 劉中民介紹。
劉中民說,《干細胞制劑制備與質檢行業標準(試行)》可以說是目前國內覆蓋干細胞種類廣、覆蓋流程全、適用范圍寬的聚焦干細胞制劑制備和質檢的行業標準,但值得一提的是,這一行業標準并非干細胞治療臨床應用的標準,僅僅只是針對干細胞制劑生產過程中的質控標準,“遵循這一標準去生產干細胞制劑,其安全性可以得到保證。”
李青峰表示:“只有獲得標準的干細胞制劑,才有可能知道可以拿它來治療什么病,而這一新發布的行業標準就是解決如何獲得符合標準的干細胞。”
李青峰指出,這一行業標準的建立,也有助于遏制社會各類虛假的干細胞美容治療手段的應用,避免屢屢有人上當受騙的局面,“在我國,干細胞制劑從未被批準應用于整形美容,如果市場上宣傳從脂肪中提取干細胞、再進行臉部注射美容的做法,那是違規的,也沒有任何科學研究的基礎,當前提取的干細胞仍然在臨床研究階段。”
劉中民同時補充說,之前媒體上被曝光的烏克蘭“干細胞特色面部美容”,號稱可以修復皮膚,就是過度宣傳,也并無科學研究的基礎。
中國整形美容協會會長張斌表示,前不久被曝光干細胞面膜引發皮膚損傷,究其原因就出在干細胞制劑的制備和質檢上,“干細胞制劑的制備和質檢影響著干細胞的質量,也關系著今后干細胞治療技術在臨床的規范應用和開展,但當前國家對于干細胞制劑的制備標準也不統一,這就導致干細胞質量參差不齊。”
尚無國家出臺統一的干細胞國家標準
張斌強調,《干細胞制劑制備與質檢行業標準(試行)》是行業共識,有助于提高干細胞制劑的產業標準,保障安全,但暫不具備法規性質,旨在為國家干細胞制劑的標準出臺提供科學基礎。
劉中民介紹說,目前,全球范圍內尚無國家出臺統一的干細胞國家標準,“國際多以美國血庫聯合會(AABB)的細胞治療板塊和國際細胞治療認證協會(FACT)的細胞處理機構標準為參考。而在國內,此前,中國醫藥生物技術協會和中國細胞生物學干細胞生物學分會從各自專業領域出發,先后發布了《干細胞制劑制備質量管理自律規范》和《干細胞通用要求》,從內容上看,仍然有值得進一步完善和細化的空間。”
而劉中民研究團隊參照國家相關管理辦法、指導原則及國際AABB標準的設計理念,結合多年來干細胞制劑制備與質檢的實踐操作經驗,起草的這一新標準涵蓋干細胞種類廣、覆蓋流程全、適用范圍寬,具有較高的參考和推廣價值。
同時,還行業標準廣泛征求了包括中國食品藥品檢定研究院袁寶珠主任、中國醫藥生物技術協會吳朝暉秘書長、中國干細胞協會籌備組組長張傳森教授等在內的近30位干細胞及相關領域權威專家的意見。
同濟大學附屬東方醫院GMP實驗室主任賈文文舉例說,每一個經過制備質檢平臺“出品”的成品干細胞都要經過一系列標準化的制備程序和10多項標準化的質檢程序。除了常規意義上的細胞采集、運輸和制備,還包括細胞鑒別、純度檢測、異常免疫學反應、生物學效力試驗等眾多環節,只有通過了層層“關卡”的干細胞成品,才能最終被平臺“放行”進入臨床研究。
賈文文介紹說,本標準在以往的標準基礎上更加細化和擴增質控標準,共有40頁,涉及11個部分,圍繞干細胞制備質檢工作所涉及各部門(機構)的職責及特點,圍繞樣本采集接收、樣本和細胞制劑運輸、樣本和干細胞制劑制備、質量檢驗控制、樣本放行和應用、細胞制劑存儲、信息管理及追溯等各環節進行了規范,為中國整形美容從業者開展干細胞臨床研究提供了規范的標準。
李青峰進一步表示,在美國,干細胞治療技術盡管不是一種藥,但因其特殊性被當做藥品一樣進行嚴格管理和規范,而我們制定這一行業標準也希望干細胞治療技術可以在國內更合理合規地開展應用,而這一標準也將會在實踐中不斷得到完善。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




