- +1
Science丨嗎啡為什么能鎮痛?從RVM到脊髓的調控網絡
嗎啡是一種廣泛使用的有效鎮痛藥,可以緩解嚴重的急性和慢性疼痛。然而,由于成癮性濫用的泛濫,嗎啡已受到了嚴格的審查。盡管嗎啡作用于多個中樞和外周的疼痛通路,但其鎮痛機制的神經解剖基礎并未完全闡明。
現有研究發現,腦干的腹內側延髓(rostral ventromedial medulla, RVM)是影響疼痛體驗的復雜大腦網絡的最終共同輸出節點。RVM損傷可以消除嗎啡鎮痛作用,而電刺激RVM則可以產生強大的鎮痛效果。這些鎮痛效果依賴于從RVM投射到脊髓的軸突束,激活從RVM投射到脊髓背角(dorsal horn)的神經元進而引起機械性鎮痛,影響疼痛信息的加工,從而調節了逃避反射的增強或抑制。這些脊髓投射神經元還控制上行傳遞的加工,從而影響疼痛的情感和感知維度。
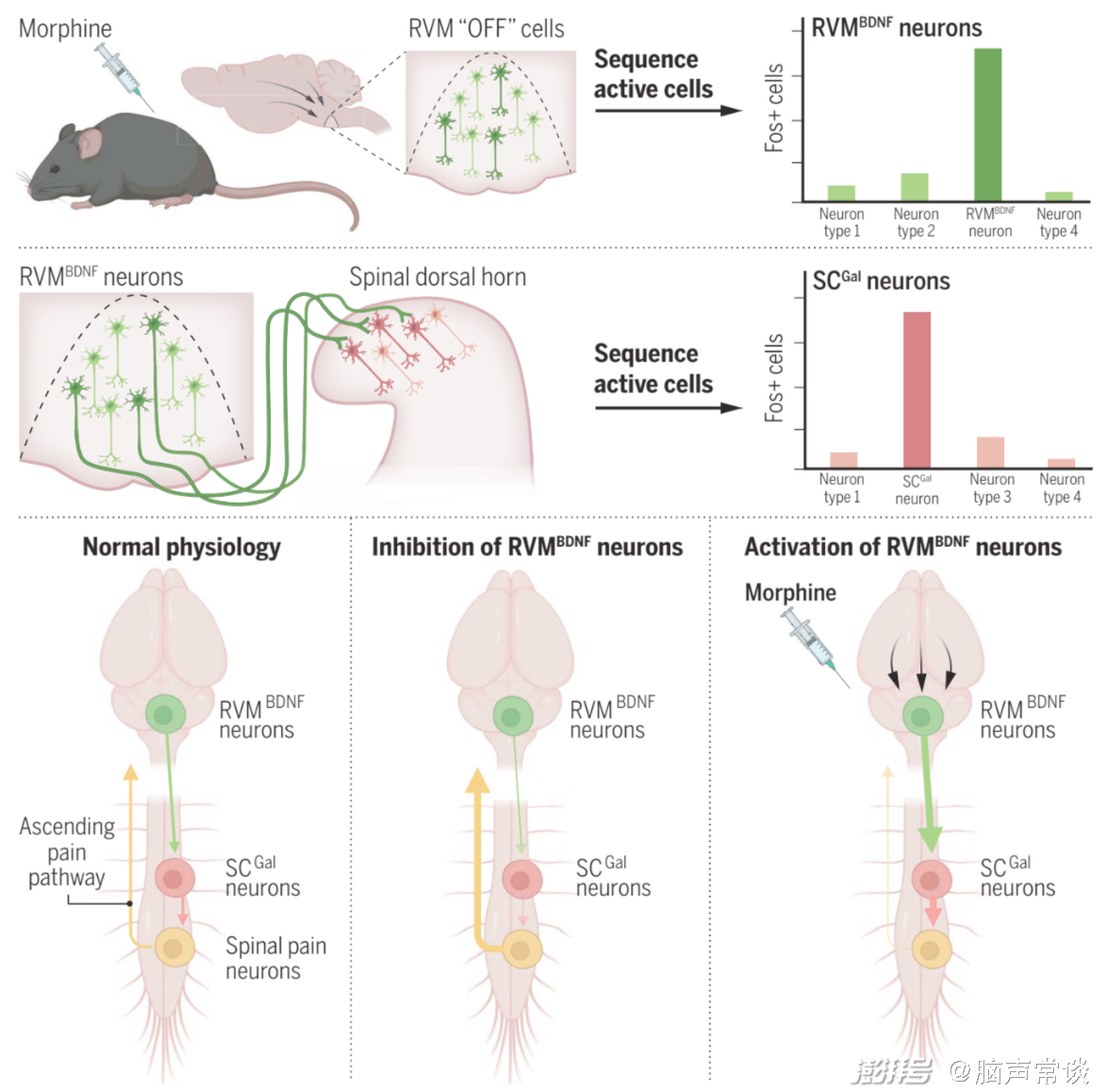
摘要圖 鑒定調節嗎啡抗傷害感受的神經元
根據RVM電刺激的強度,疼痛感受可以被增強或抑制。RVM中的5-羥色胺能神經元、GABA能神經元,甚至可能還有谷氨酸能神經元都參與了疼痛的調節。疼痛刺激與某些RVM神經元活動的增強或降低相關。嗎啡鎮痛所依賴的μ型阿片受體廣泛存在于參與疼痛體驗的所有神經底物中,實驗證據也支持脊髓和多個腦區在鎮痛中的參與。因此,RVM下行抑制對上行傳遞的相對貢獻以及其中涉及的機制,一直是理解阿片類藥物鎮痛作用的一個重要問題。
8月30日,卡羅林斯卡醫學院的Patrik Ernfors團隊在Science雜志上發表論文Morphine-responsive neurons that regulate mechanical antinociception,探究嗎啡誘導的機械性止痛在小鼠中的神經機制,發現了一組特定的神經元集群在RVM中對嗎啡有反應,并在調節機械性疼痛敏感性中起關鍵作用。

圖源:Science
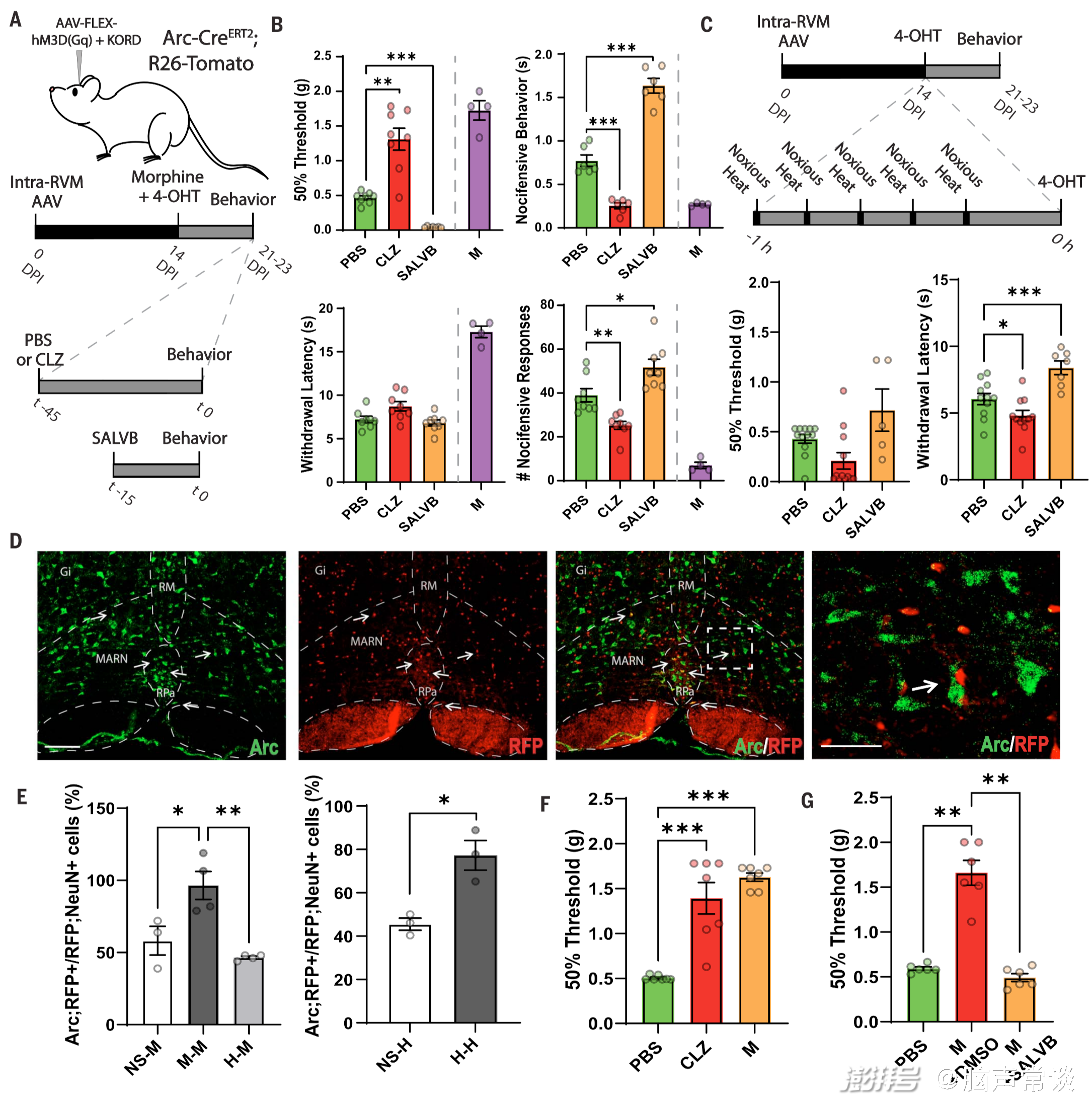
圖1 RVM中的嗎啡抗疼痛集合體
研究團隊通過轉基因小鼠實驗發現了一組位于RVM中的神經元RVMBDNF,它們在調節機械性疼痛方面起著關鍵作用,并且對嗎啡刺激具有反應。這些神經元屬于一個特定的神經回路(RVM-脊髓回路),該回路可以調節機械性疼痛的感知,并賦予嗎啡其鎮痛特性。通過強制激活或抑制這些RVMBDNF神經元,研究人員可以模擬嗎啡誘導的機械性鎮痛效果,而抑制它們則可以完全逆轉嗎啡誘導的機械性鎮痛,這一過程依賴于BDNF/TrkB信號通路,并且是通過激活脊髓上的抑制性神經元(galanin-positive neurons)來實現。研究人員通過,發現激活RVM中的嗎啡反應性神經元可以增加脊髓背角淺層的神經元活性,而抑制這些脊髓神經元則可以完全消除RVM神經元激活或嗎啡導致的機械性鎮痛效果。
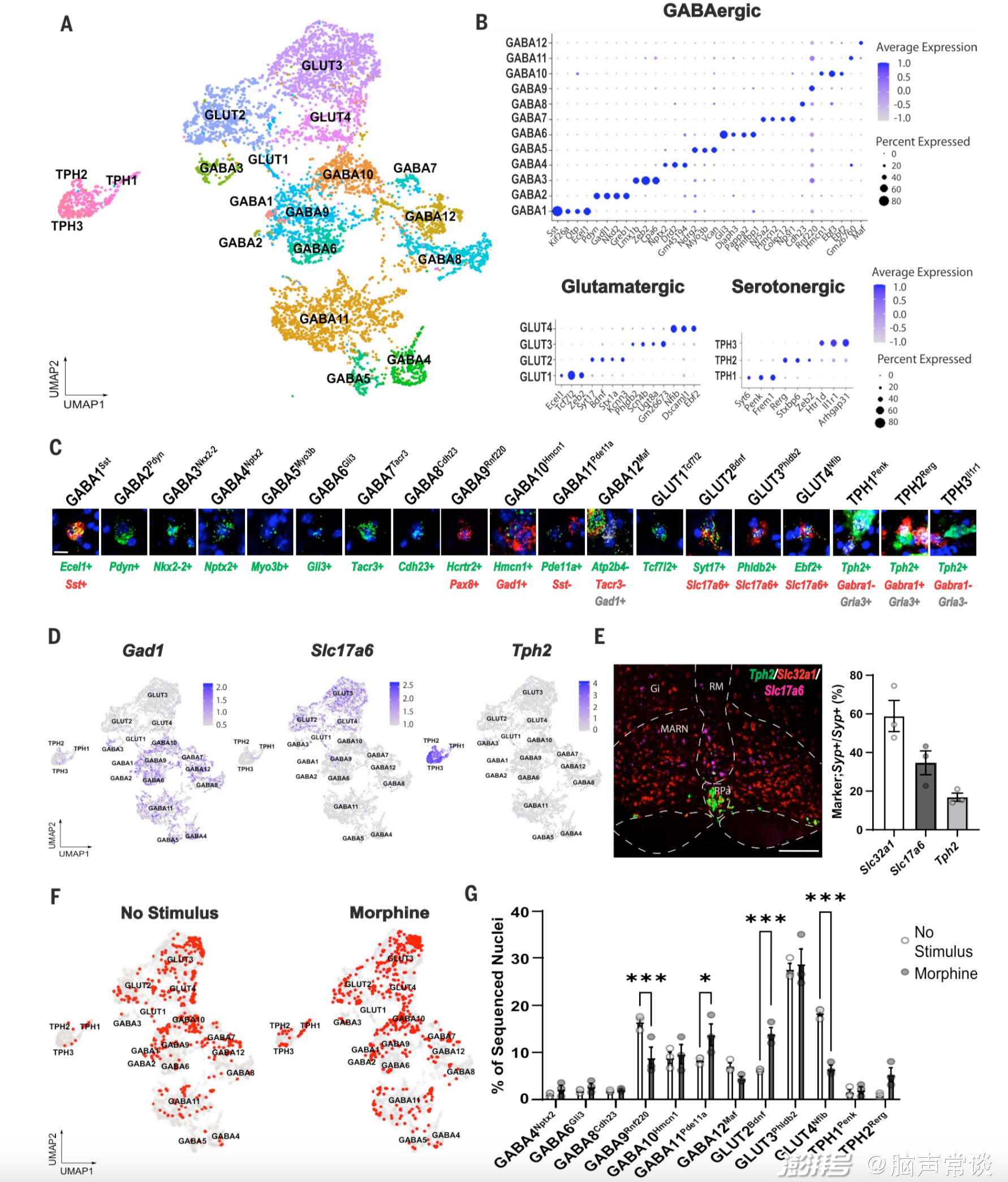
圖2 嗎啡抗疼痛效應相關的RVM神經元群體的分子特征
在進一步的驗證中,研究人員結合TRAP和CANE(capturing activated neuronal ensembles)技術,發現通過激活RVM中的谷氨酸能神經元可以增加脊髓背角淺層神經元的活性,而這些脊髓神經元在介導鎮痛效果中起關鍵作用;而抑制這些脊髓神經元可以完全消除RVM神經元激活或嗎啡導致的鎮痛效果,表明RVM中的谷氨酸能神經元在介導嗎啡鎮痛中起關鍵作用。單細胞轉錄組分析也進一步揭示這個結論,這些從RVM投射到脊髓的神經元包括抑制性神經元(GABAergic和serotonergic)以及少量的興奮性神經元(glutamatergic),主要包含三種投射到脊髓的神經元類型:抑制性神經元、谷氨酸能神經元和少量的5-羥色胺能神經元。其中,谷氨酸能GLUT2神經元是RVM中對嗎啡最敏感的神經元類型,在介導鎮痛效果中起關鍵作用。而RVMBDNF神經元便是主要屬于谷氨酸能神經元類型,RVMBDNF神經元中的一部分會投射到脊髓,通過脊髓向大腦傳遞感覺信息通路,從而影響機械性疼痛的感知。當使用化學遺傳學方法激活這些BDNF神經元時,可以觀察到脊髓中Excitatory 20(Ex20)和Inhibitory 8(In8)神經元的活性增加,表現為即時早基因(immediately early gene, IEG)表達的上調。這表明,RVMBDNF神經元可以通過激活脊髓中特定的興奮性和抑制性神經元來產生鎮痛作用。
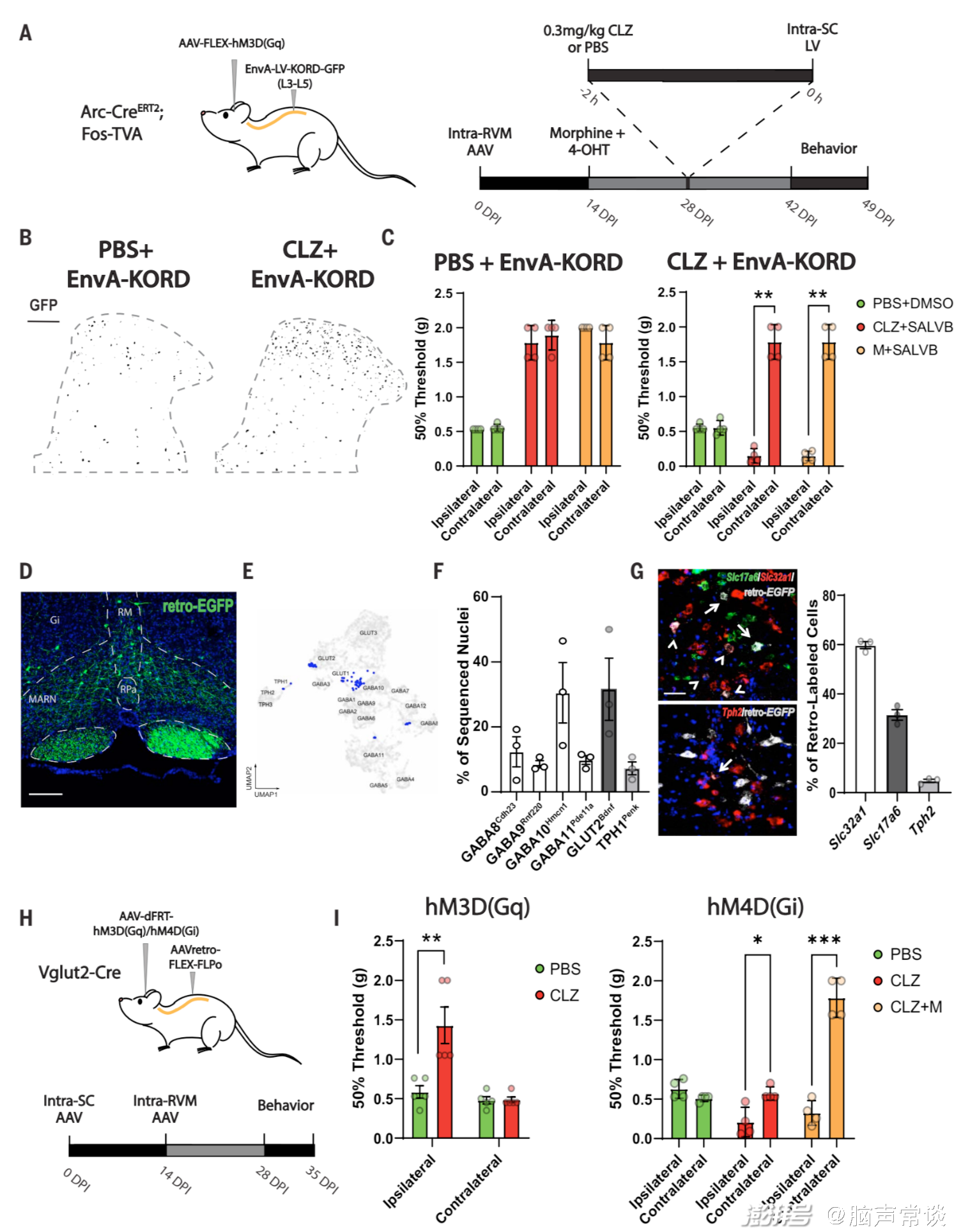
圖3 嗎啡引發的止痛作用是通過激活脊髓的興奮性RVM神經細胞來實現的
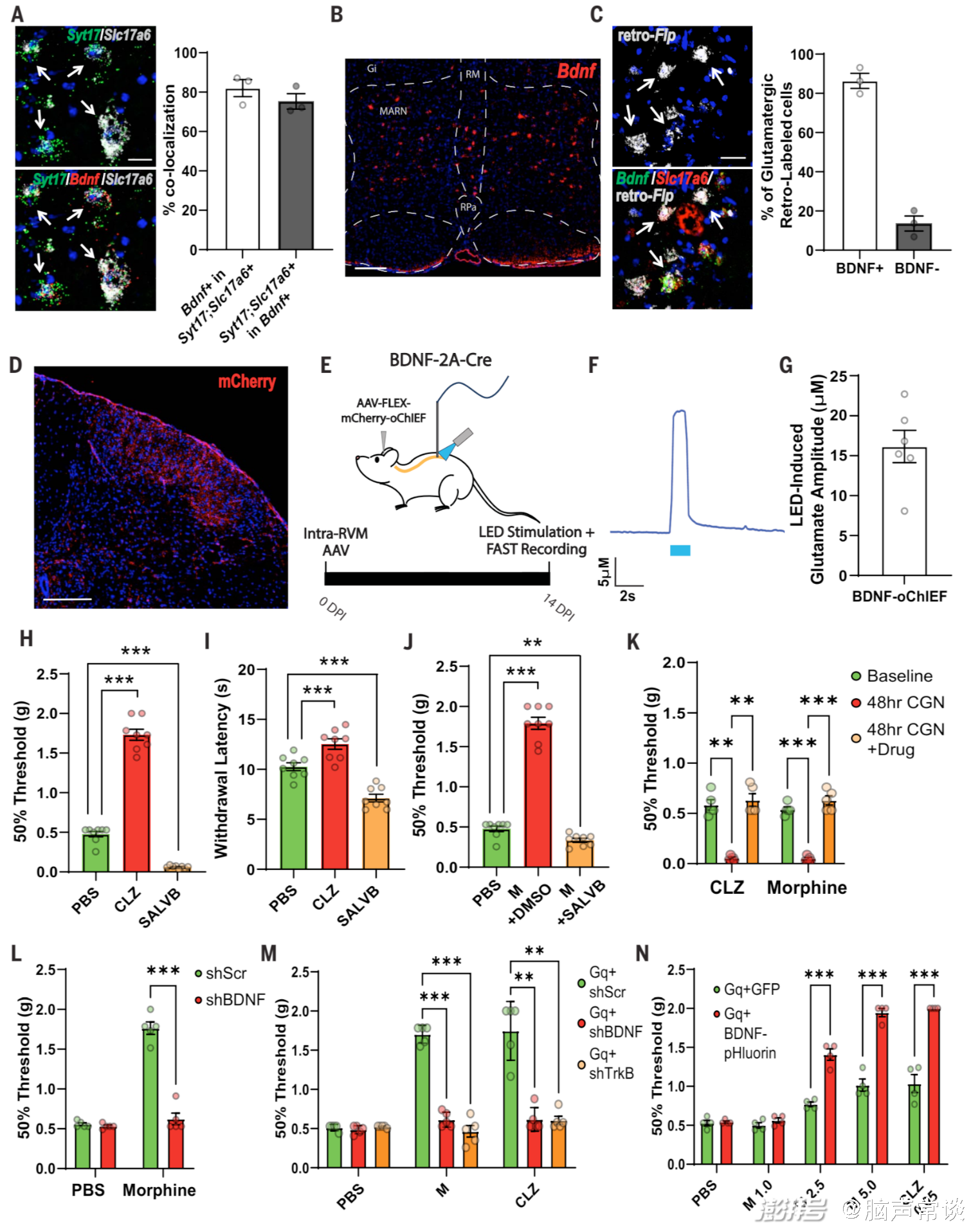
圖4 RVMBDNF神經元介導的嗎啡抗疼痛作用依賴于BDNF/TrkB
最后研究人員利用FAST(fast analytical sensing technology)技術結合光遺傳學等方法,對神經元谷氨酸釋放的動力學特征進行了檢測。將光敏感離子通道蛋白oChIEF(Cre-dependent ChR2 variant)表達在目標神經元上,并用用藍光刺激oChIEF表達的神經元軸突末梢,誘發谷氨酸的釋放。然后在脊髓L4-L5區域植入微電極陣列,通過施加固定電位,可以檢測到谷氨酸被氧化產生的電流變化,從而測量谷氨酸的濃度變化。研究人員通過分析谷氨酸濃度的最大振幅和80%的衰減時間,用以評估神經元活動的動力學特征。他們還通過數據分析,評估了不同神經元亞群在基線和給藥條件下的活動變化,從而探究了神經元活動與疼痛感知的關系。這種結合光遺傳學、電生理和生物信息學的多模態方法,為深入理解疼痛調控機制提供了新的研究思路。
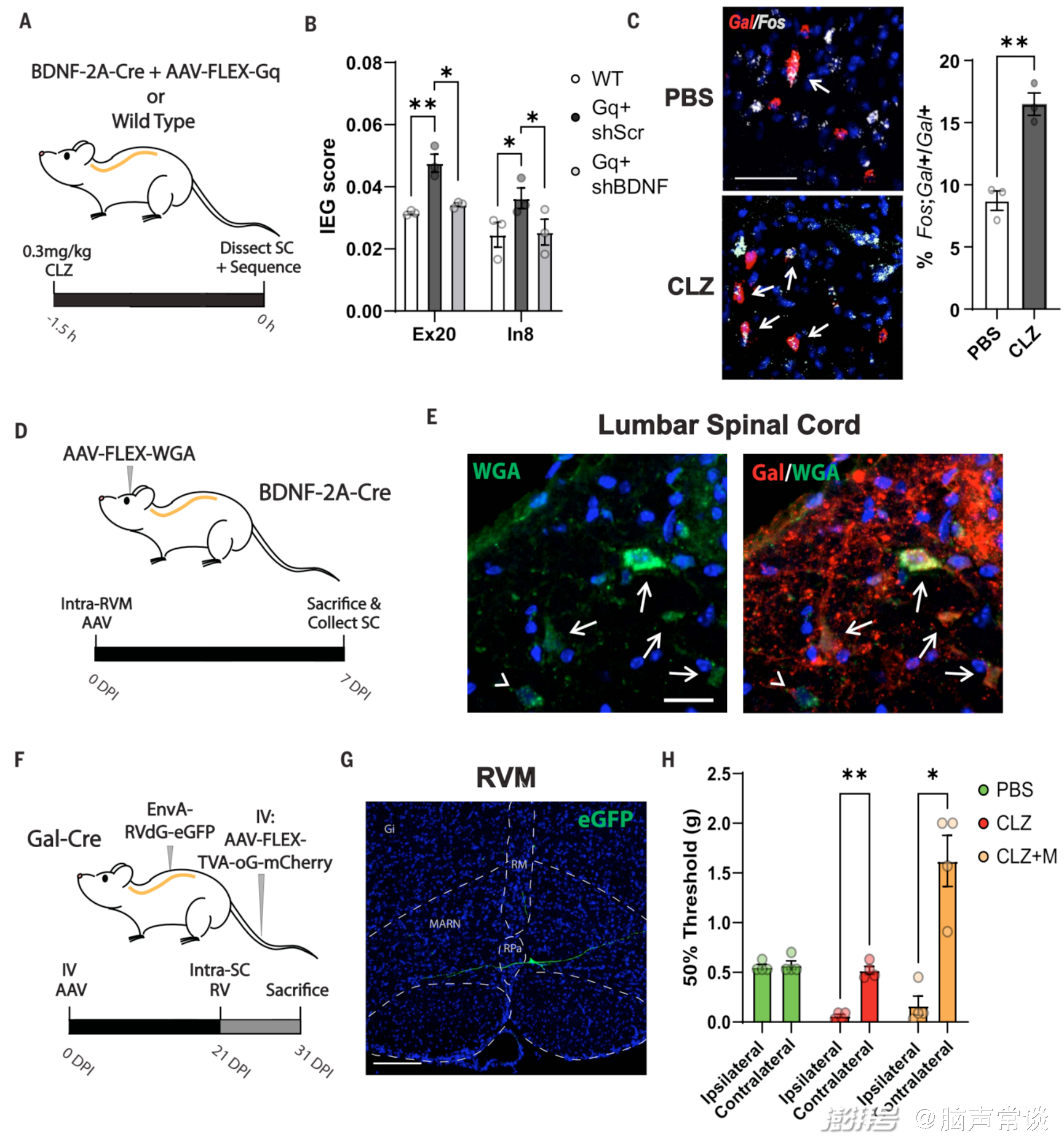
圖5 嗎啡在脊髓中的止痛機理
在該項研究中,該團隊采用了多種實驗手段,包括基因操控、行為學測試、病毒注射和組織學分析等,旨在從神經元活動的角度深入探究疼痛機制。首先,研究人員使用了多種轉基因小鼠模型,包括Arc-CreERT2、Vglut2-Cre和BDNF-2A-Cre小鼠,通過基因操控標記和操控特定神經元群體,同時使用Gal-Cre轉基因小鼠和C57BL/6J野生型小鼠作為對照。為了評估小鼠對熱刺激和機械性刺激的反應,研究人員采用了Hargreaves熱刺激實驗、熱板實驗和胡椒素注射實驗等行為學測試。此外,研究人員還進行了病毒注射實驗,包括腦內注射、脊髓注射和靜脈注射,利用不同病毒載體(AAV、EnvA-pseudotyped等)轉染特定神經元群體,以操控和標記它們。為了檢測和定量特定蛋白(如Arc、NeuN)在腦區和脊髓中的表達情況,研究人員采用了免疫熒光染色和定量分析實驗,以評估神經元的活性和分布。最后,研究人員利用FAST技術測量神經元釋放谷氨酸的動力學特征,以探究神經元活動與疼痛感知的關系;并采用免疫熒光染色和定量分析實驗,以評估神經元的活性和分布。
熱板實驗是一種常用于評估小鼠對熱刺激的反應的行為學實驗方法。在這個實驗中,小鼠被放置在一個正方形的透明塑料箱中,直接放在一個設定溫度為48°C的熱板上。實驗人員會記錄小鼠在2分鐘內出現舔舐、咬咬、抖動等逃避反應的次數。這種熱刺激可以引起小鼠的疼痛感知反應,從而評估其熱覺敏感性。除了熱板實驗,研究人員還使用了Hargreaves熱刺激實驗來評估小鼠的熱覺敏感性。研究團隊利用Hargreaves熱刺激實驗用以評估小鼠的熱覺敏感性。他們首先將小鼠放置在一個透明的塑料箱中,箱底為玻璃板,玻璃板下方放置一個輻射熱源,用于照射小鼠的后爪。實驗人員記錄小鼠后爪出現逃避反應的時間,每只小鼠刺激3次,間隔2分鐘。研究人員使用Arc-CreERT2小鼠用以捕獲對嗎啡和熱刺激反應的神經元,他們首先給小鼠皮下注射10 mg/kg的嗎啡,75分鐘后注射50 mg/kg的4-羥基他莫昔芬(4-OHT),以此尋找嗎啡激活的神經元。為了捕獲熱刺激反應的神經元,研究人員使用Hargreaves裝置刺激小鼠的一只后爪,直到其出現逃避反應,重復5次,每次間隔10分鐘,并在20分鐘后,小鼠也被注射50 mg/kg的4-OHT。通過熱板實驗和Hargreaves實驗,研究人員可以了解小鼠對熱刺激的行為反應,為進一步探究疼痛感知的神經機制提供重要依據。這些行為學實驗方法是神經科學研究中常用的工具,有助于揭示疼痛調控的神經生物學基礎。
結論與展望
研究發現,RVM區域存在一群特定的神經元,它們對嗎啡的刺激能作出鎮痛反應。通過單細胞轉錄組學分析,研究者鑒定出這些神經元的分子特征,并發現其中部分興奮性神經元表達BDNF。進一步的實驗證明,強制激活這些RVMBDNF神經元可以模擬嗎啡誘導的機械性鎮痛效果,而抑制它們則可以完全逆轉這一效果。這些結果表明,RVMBDNF神經元通過釋放BDNF,激活脊髓抑制性神經元,從而調節機械性疼痛信號的傳遞,是嗎啡鎮痛的關鍵神經回路。此外,這項研究還采用了多種先進的技術手段,如單細胞轉錄組學、光遺傳學、快速電化學檢測等,為探索復雜神經系統功能提供了新的研究范式。例如,通過單細胞轉錄組學分析RVM區域的神經元亞群,得以成功鑒定出調控機械性鎮痛的關鍵神經元群體。利用光遺傳學技術可以精準地操控這些神經元的活性,從而揭示其在嗎啡鎮痛中的作用。此外,快速電化學檢測技術還能實時監測脊髓內谷氨酸的動態變化,為理解神經遞質調控機制提供了新的研究手段。這些創新性的技術手段為神經科學研究開辟了新的可能性。
這一發現不僅豐富了我們對嗎啡鎮痛機制的理解,也為開發新的鎮痛藥物提供了新的靶點。通過精準調控RVM-脊髓這一關鍵神經回路,有望設計出新一代更加有效且安全的鎮痛藥物,減少嗎啡等傳統阿片類藥物的副作用。
本文為澎湃號作者或機構在澎湃新聞上傳并發布,僅代表該作者或機構觀點,不代表澎湃新聞的觀點或立場,澎湃新聞僅提供信息發布平臺。申請澎湃號請用電腦訪問http://renzheng.thepaper.cn。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




