- +1
這款乳腺癌新藥,或使受益人群從20%提高至50%
·Trastuzumab Deruxtecan在2022年5月被中國(guó)藥監(jiān)局納入優(yōu)先審批行列,距今不到一年就獲批。甚至在藥監(jiān)局審批前,2022年2月就落戶海南博鰲樂(lè)城國(guó)際醫(yī)療旅游先行區(qū)。這次中國(guó)獲批的還是HER2陽(yáng)性乳腺癌,但HER2低表達(dá)乳腺癌的上市申請(qǐng)也已被藥監(jiān)局受理。我們可以看到近年來(lái)很多對(duì)患者幫助極大的創(chuàng)新藥的軌跡:國(guó)內(nèi)外上市的時(shí)間差不斷縮短。此外,國(guó)內(nèi)也有大量的抗體偶聯(lián)藥屬于研發(fā)狀態(tài),在技術(shù)層面的創(chuàng)新也在與國(guó)外逐漸同步。
Trastuzumab Deruxtecan(德曲妥珠)。
2月24日,中國(guó)國(guó)家藥品監(jiān)督管理局(NMPA)批準(zhǔn)了阿斯利康和第一三共聯(lián)合開(kāi)發(fā)的抗體偶聯(lián)藥物Trastuzumab Deruxtecan(德曲妥珠)在過(guò)往治療耐藥的HER2陽(yáng)性乳腺癌患者中使用。
每年獲批上市的新藥有很多,但Trastuzumab Deruxtecan絕非一個(gè)平平無(wú)奇的新藥。在2022年6月5日,匯聚全球腫瘤領(lǐng)域精英的美國(guó)臨床腫瘤學(xué)會(huì)年會(huì)上,它的一個(gè)乳腺癌三期臨床試驗(yàn)報(bào)告獲得全場(chǎng)起立鼓掌的特殊待遇。這可以說(shuō)是極為罕見(jiàn)的殊榮。
Trastuzumab Deruxtecan憑什么獲得了這種區(qū)別對(duì)待?這是因?yàn)閺尼t(yī)學(xué)角度,它重新定義了乳腺癌治療的格局;從藥物研發(fā)角度,它代表了抗體偶聯(lián)這一整個(gè)藥物技術(shù)平臺(tái)的突破。

2月24日,國(guó)家藥品監(jiān)督局管理局發(fā)布的藥品批準(zhǔn)證明文件送達(dá)信息截圖。
在乳腺癌分類(lèi)與治療基石上的超越
乳腺癌是女性最常見(jiàn)的惡性腫瘤。據(jù)世界衛(wèi)生組織統(tǒng)計(jì),2020年全球就有230萬(wàn)女性確診乳腺癌,死亡人數(shù)達(dá)68.5萬(wàn)。乳腺癌在中國(guó)的發(fā)生率、死亡率也一直處于上升狀態(tài)。在可預(yù)見(jiàn)的將來(lái),乳腺癌都會(huì)是中國(guó)以及全世界極大的健康負(fù)擔(dān)。
不過(guò)乳腺癌預(yù)后也有了長(zhǎng)足進(jìn)展。美國(guó)2010年后的數(shù)據(jù)顯示,相對(duì)健康人,乳腺癌患者5年的存活率是90%[3]。能有這么高的存活率,主要貢獻(xiàn)因素有兩個(gè),一是有效的篩查讓更多患者在早期就被確診,二是針對(duì)不同類(lèi)型乳腺癌有了更多有效的治療手段。就后者而言,乳腺癌如今分類(lèi)與治療上起決定因素的是腫瘤細(xì)胞HER2與激素受體(HR)的表達(dá)狀況。
如果乳腺癌患者腫瘤有HR表達(dá),往往意味著腫瘤細(xì)胞的增殖依賴激素,激素阻斷可作為治療手段。而當(dāng)乳腺癌腫瘤細(xì)胞表達(dá)HER2時(shí),則可以利用靶向HER2的抗體藥來(lái)殺死腫瘤細(xì)胞。第一個(gè)HER2抗體藥,也是HER2陽(yáng)性乳腺癌治療的基石,就是曲妥珠單抗(Trastuzumab)。
曲妥珠單抗在1992年進(jìn)入人體試驗(yàn),到1996年時(shí)臨床試驗(yàn)已擴(kuò)展到900人,但由于該藥聲名在外,迫于社會(huì)壓力,藥企與FDA不得不允許每季度抽簽1000名患者在臨床試驗(yàn)外獲得該藥物的使用。自1998年被FDA批準(zhǔn)后,它對(duì)乳腺癌的治療、預(yù)后都產(chǎn)生了巨大的影響。如果不考慮治療手段,HER2陽(yáng)性的乳腺癌相較HER2陰性乳腺癌惡性程度更高,預(yù)后也更差。可是曲妥珠單抗上市后,大幅改善了HER2陽(yáng)性乳腺癌的預(yù)后,如今HER2陽(yáng)性乳腺癌反而成了預(yù)后最好的類(lèi)型。曲妥珠單抗僅原研藥如今已惠及的病人超過(guò)230萬(wàn),可以說(shuō)在乳腺癌甚至整個(gè)腫瘤治療領(lǐng)域都是具有革命意義的創(chuàng)新。
但只有HER2陽(yáng)性的病人才能從曲妥珠單抗等HER2靶向藥中獲益,而這只是乳腺癌患者中的一小部分——HER2陽(yáng)性的乳腺癌患者不到所有病人的20%:
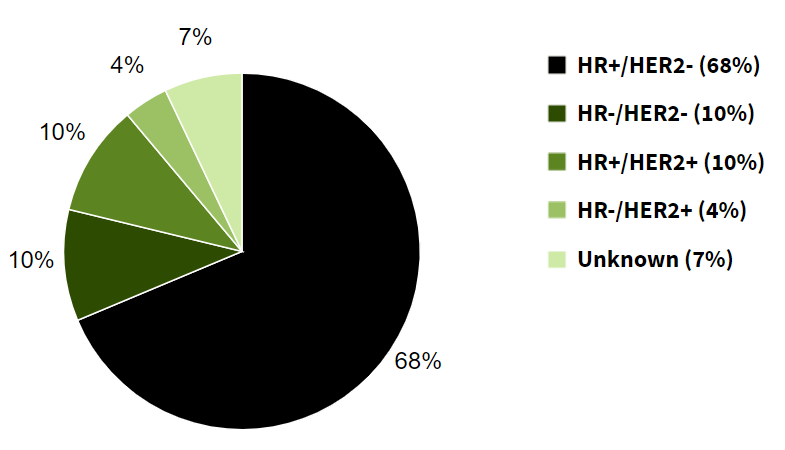
附圖1.乳腺癌患者各分型占比(美國(guó)2015-2019數(shù)據(jù))
絕大多數(shù)患者并沒(méi)有機(jī)會(huì)從HER2靶向藥中獲益。特別是三陰性乳腺癌(HR-/HER2-),很多人可能也聽(tīng)說(shuō)過(guò)這類(lèi)乳腺癌是最麻煩的。確實(shí)三陰性乳腺癌適用的治療藥物很少,一旦到了遠(yuǎn)端轉(zhuǎn)移階段,5年相對(duì)存活率只有12%,遠(yuǎn)遠(yuǎn)低于HR+/HER2+的46%與HR-/HER2+的38.8%。
但與一般人的印象不同,HER2陰性不是說(shuō)癌細(xì)胞沒(méi)有表達(dá)HER2,只是說(shuō)HER2表達(dá)的量沒(méi)有到一個(gè)很高的程度。例如目前使用HER2表達(dá)鑒定標(biāo)準(zhǔn),結(jié)合了蛋白質(zhì)表達(dá)與基因水平表達(dá)。其中蛋白質(zhì)表達(dá)采用IHC技術(shù),只有在0-3分的打分系統(tǒng)里達(dá)到3分,或者是2分同時(shí)基因表達(dá)陽(yáng)性,才是HER2陽(yáng)性,否則一律陰性——包括了很多有HER2表達(dá),只是不那么高的情況。
可能有人會(huì)好奇,為何如此苛刻,標(biāo)準(zhǔn)放松點(diǎn),讓更多病人用上HER2靶向藥不好嗎?確實(shí)不好。因?yàn)樵囘^(guò)了,沒(méi)用。這種沒(méi)用還不僅是乳腺癌里的問(wèn)題。聽(tīng)到HER2,大家第一反應(yīng)都是乳腺癌,其實(shí)HER2在別的腫瘤里也是有表達(dá)的,為什么沒(méi)怎么聽(tīng)說(shuō)呢?因?yàn)橹耙苍囘^(guò),除了極少數(shù)情況外還是沒(méi)用,這很可能是由于相較乳腺癌,其它腫瘤的HER2表達(dá)即使有也低很多。
明明有HER2表達(dá),而且HER2靶向藥在HER2陽(yáng)性患者里還有非常好的療效,這讓科學(xué)家與藥企們對(duì)只能把HER2靶向藥用于HER2陽(yáng)性患者非常不甘心。曲妥珠單抗面世后,很多制藥公司都在嘗試做一個(gè)更好的HER2靶向藥。
有的在做一個(gè)更好的HER2單抗藥。曲妥珠單抗是20世紀(jì)90年代的產(chǎn)品,那時(shí)候制作抗體藥的技術(shù)遠(yuǎn)不如當(dāng)下先進(jìn)。曲妥珠單抗對(duì)HER2腫瘤的抗癌作用依賴抗體與HER2結(jié)合,刺激免疫細(xì)胞殺傷被抗體標(biāo)識(shí)出來(lái)的癌細(xì)胞也是潛在作用機(jī)理之一。因此就有藥企嘗試抗體改造,做一個(gè)與HER2結(jié)合能力更強(qiáng),刺激免疫細(xì)胞殺傷能力也更強(qiáng)的單抗。
抗體偶聯(lián)藥——換一種思路
另一種思路是抗體偶聯(lián)藥,在HER2抗體上加一個(gè)細(xì)胞毒性藥物(如化療藥物),讓細(xì)胞毒性藥物助力單抗,成為對(duì)HER2表達(dá)腫瘤殺傷力更強(qiáng)的藥物,能克服“HER2表達(dá)量不夠高”這一攔路虎。
不過(guò)以往這些嘗試只在解決曲妥珠單抗的耐藥性上取得了有限的成功。比如在曲妥珠基礎(chǔ)上開(kāi)發(fā)的抗體偶聯(lián)藥物Trastuzumab Emtansine,HER2陽(yáng)性的患者對(duì)曲妥珠耐藥后,這個(gè)藥還能起效。這類(lèi)進(jìn)展對(duì)患者來(lái)說(shuō)仍然有積極意義,可是沒(méi)有讓更多因HER2表達(dá)不夠高而沒(méi)法用HER2靶向藥的患者受益。
直到Trastuzumab Deruxtecan這個(gè)抗體偶聯(lián)藥橫空出世。從名字可知,作為抗體偶聯(lián)藥物,Trastuzumab Deruxtecan靶向HER2的抗體部分還是1998年就上市的曲妥珠單抗,在此之上又加上了細(xì)胞毒性藥物Deruxtecan。
2019年末,F(xiàn)DA先批準(zhǔn)了Trastuzumab Deruxtecan在接受過(guò)往HER2靶向治療后耐藥的HER2陽(yáng)性乳腺癌患者中的使用。在相關(guān)的臨床試驗(yàn)中,受試者至少接受過(guò)兩種以及更多HER2靶向治療后發(fā)生耐藥。可就在這樣的人群里,Trastuzumab Deruxtecan仍然有很好的療效,總體應(yīng)答率達(dá)到了60.3%。之后在更早期的HER2陽(yáng)性病人中,Trastuzumab Deruxtecan也展示了比Trastuzumab emtansine更好的療效,成了曲妥珠耐藥后的新標(biāo)準(zhǔn)療法。
在一系列的驚人成功后,越來(lái)越多的人開(kāi)始相信Trastuzumab Deruxtecan不僅是一個(gè)加強(qiáng)版曲妥珠單抗,曾經(jīng)限制HER2靶向藥的種種難題——包括HER2的表達(dá)量,或許可以被Trastuzumab Deruxtecan突破。
而在2022年6月5日,一項(xiàng)名為DESTINY-Breast04的臨床試驗(yàn)結(jié)果在美國(guó)臨床腫瘤學(xué)會(huì)年會(huì)上公布,在該試驗(yàn)中,HER2陽(yáng)性這一HER2靶向藥的限制因素終于被Trastuzumab Deruxtecan徹底擊穿。
DESTINY-Breast04試驗(yàn)中的受試者都是HER2低表達(dá)的轉(zhuǎn)移期乳腺癌患者。試驗(yàn)中,采用現(xiàn)今的標(biāo)準(zhǔn)療法化療的患者們,腫瘤無(wú)進(jìn)展生存時(shí)間是5個(gè)月,而Trastuzumab Deruxtecan組直接延長(zhǎng)了快一倍,接近10個(gè)月。化療組的總體生存時(shí)間是16.8個(gè)月,Trastuzumab Deruxtecan組接近兩年。
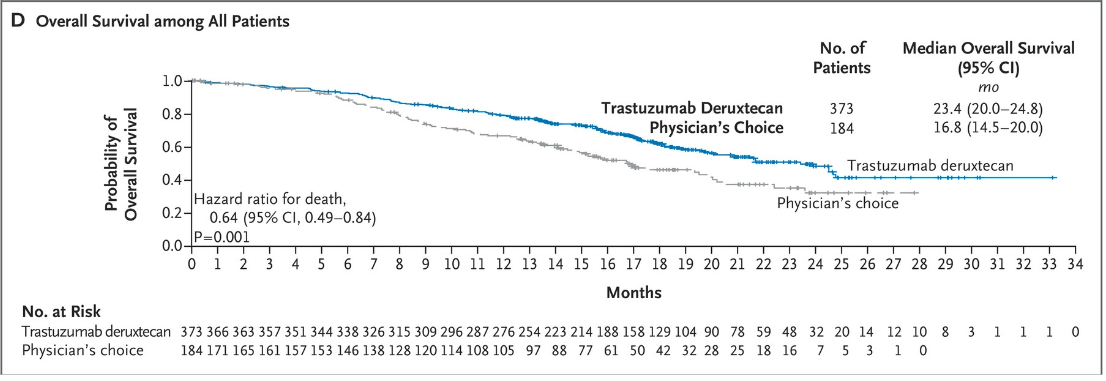
附圖2. Trastuzumab Deruxtecan顯著延遲了HER2地表達(dá)患者的生存時(shí)間
這些結(jié)果意味著采用Trastuzumab Deruxtecan治療,患者疾病惡化的風(fēng)險(xiǎn)下降了近一半,生存時(shí)間也大幅延長(zhǎng)。
這些HER2低表達(dá)患者到底是多低的HER2表達(dá)呢?從HER2表達(dá)的傳統(tǒng)鑒定中,DESTINY-Breast04試驗(yàn)中的受試者要么是HER2蛋白表達(dá)只有1,或者蛋白表達(dá)有2分但基因表達(dá)陰性。這些受試者在當(dāng)下的乳腺癌分類(lèi)中要么屬于HR陽(yáng)性HER2陰性,要么屬于三陰性。90%的受試者接受過(guò)至少兩線治療,可以說(shuō)這是一個(gè)經(jīng)歷過(guò)多種治療后耐藥,已經(jīng)沒(méi)有什么選擇的患者群體。該結(jié)果可以說(shuō)是出人意料的好。伴隨這一突破性的進(jìn)展,乳腺癌患者中HER2低表達(dá)人群不必再歸于HER2陰性,她們是一個(gè)新的獨(dú)立分類(lèi),Trastuzumab Deruxtecan將成為她們的新標(biāo)準(zhǔn)療法。
HER2低表達(dá)的乳腺癌患者有多少呢?80%的乳腺癌患者是HER2陰性,但里面超過(guò)60%是有HER2表達(dá)。也就是說(shuō)Trastuzumab Deruxtecan讓HER2靶向藥適用人群從原來(lái)的不到20%的HER2陽(yáng)性人群,一下子增加到了一半以上的乳腺癌患者。
伴隨著Trastuzumab Deruxtecan,我們正在見(jiàn)證乳腺癌,這一女性中發(fā)病率最高的癌癥,從分類(lèi)與治療都將發(fā)生翻天覆地的變化。也正是因?yàn)檫@樣重大的意義,當(dāng)研究人員公布DESTINY-Breast04試驗(yàn)結(jié)果時(shí),即便是見(jiàn)慣了新藥試驗(yàn)結(jié)果公布的美國(guó)臨床腫瘤學(xué)會(huì)年會(huì)參與者們也忍不住起立鼓掌致意。
抗體偶聯(lián)藥物終獲突破
2022年8月5日,F(xiàn)DA批準(zhǔn)了Trastuzumab Deruxtecan在HER2低表達(dá)乳腺癌患者中的使用,正式開(kāi)啟了乳腺癌的分類(lèi)與治療的變革。可是這一重大革新的背后絕非一帆風(fēng)順,Trastuzumab Deruxtecan的技術(shù)平臺(tái)——抗體偶聯(lián)藥物,曾經(jīng)被寄予厚望,又屢次給出讓人失望的結(jié)果。可以說(shuō),直到Trastuzumab Deruxtecan的出現(xiàn),抗體偶聯(lián)藥物才獲得了真正的“正名”。這也是為什么我們說(shuō)Trastuzumab Deruxtecan在藥物研發(fā)方面,代表了一個(gè)技術(shù)平臺(tái)的突破。
抗體偶聯(lián)藥物的概念可以追溯到諾貝爾獎(jiǎng)得主Paul Ehrlich在1907提出的“神奇子彈”理論——如果可以將一個(gè)毒性物質(zhì)非常專(zhuān)一地遞送到病灶處,那么將可以清除病灶而不影響身體其它部分。在抗體偶聯(lián)藥這個(gè)技術(shù)平臺(tái)里,我們正是希望利用抗體的特異性,例如只與腫瘤細(xì)胞結(jié)合的抗體,將毒性藥物僅僅送到腫瘤里。
當(dāng)2001年全球第一個(gè)抗體偶聯(lián)藥——用于復(fù)發(fā)型急性髓細(xì)胞白血病的Gemtuzumab Ozogamicin被FDA以加速審批上市批準(zhǔn)上市后,制藥界對(duì)抗體偶聯(lián)藥充滿了希望,認(rèn)為Ehrlich的“神奇子彈”即將通過(guò)抗體偶聯(lián)藥在癌癥治療里廣泛使用。可接下來(lái)迎接抗體偶聯(lián)藥的不是對(duì)癌癥治療的變革,而是無(wú)數(shù)次失望。
研究人員很快就發(fā)現(xiàn)抗體偶聯(lián)藥一點(diǎn)都不像Ehrlich提出的只殺病灶不損傷健康組織的“神奇子彈”。很多抗體偶聯(lián)藥的不良反應(yīng)非常大,甚至都難以在有效劑量與毒性劑量間找到一個(gè)治療窗口。Gemtuzumab Ozogamicin這個(gè)抗體偶聯(lián)藥的老大,因?yàn)槎拘蕴笥譀](méi)有在后續(xù)試驗(yàn)驗(yàn)證有效性,還在2010年黯然退市,直到2017年換了一個(gè)病人群體重新做試驗(yàn),再降低了劑量才得以回歸使用。
為什么會(huì)出現(xiàn)如此大的落差?這或許是由于抗體偶聯(lián)藥的復(fù)雜性被大大低估了。抗體偶聯(lián)藥的三個(gè)組成:抗體、載藥(如化療藥物)以及連接二者的鏈接,制藥業(yè)曾經(jīng)認(rèn)為只要把這三個(gè)湊到一起,一個(gè)毒藥就能被專(zhuān)一地送到腫瘤里,萬(wàn)事大吉。可現(xiàn)實(shí)是很少有只在腫瘤里表達(dá)的抗原,因此一個(gè)靶向腫瘤的“特異性”抗體多少也會(huì)跑到健康組織。鏈接與載藥也不是原先預(yù)想的簡(jiǎn)單的化學(xué)小分子,而是需要仔細(xì)考量其穩(wěn)定性與作用機(jī)理。比如鏈接的穩(wěn)定性問(wèn)題,是必須在細(xì)胞內(nèi)釋放載藥好,還是不必嚴(yán)格在細(xì)胞內(nèi)只要在腫瘤組織內(nèi)釋放就行,這里面就大有學(xué)問(wèn)。
在抗體偶聯(lián)藥因早期的失望陷入低谷,不少藥企紛紛削減投入之際,這一技術(shù)平臺(tái)卻開(kāi)始了臥薪嘗膽之旅。揀選抗體與載藥,研發(fā)不同鏈接,最終有了以Trastuzumab Deruxtecan為代表的全新一代抗體偶聯(lián)藥。
可以與早期的HER2抗體偶聯(lián)藥Trastuzumab Emtansine對(duì)比,后者平均每個(gè)抗體分子上只有3.5個(gè)細(xì)胞毒性藥物Emtansine,而Trastuzumab Deruxtecan上每個(gè)抗體分子連著8個(gè)Deruxtecan。連接Trastuzumab與Deruxtecan的鏈接是可剪切的,意味著不用進(jìn)入腫瘤細(xì)胞,鏈接就可以被打破,釋放出來(lái)的載藥Deruxtecan殺傷腫瘤細(xì)胞的同時(shí)還可能起了刺激周?chē)?xì)胞的作用。Deruxtecan又屬于未在乳腺癌中使用過(guò)的化療藥物類(lèi)型,可能帶來(lái)了與以往乳腺癌治療不同的新機(jī)理。
正是依賴抗體偶聯(lián)藥整個(gè)技術(shù)平臺(tái)過(guò)去多年來(lái)各種細(xì)微創(chuàng)新的積累,才有可能在今天出現(xiàn)Trastuzumab Deruxtecan這樣一個(gè)能以一己之力改變最常見(jiàn)、社會(huì)影響與負(fù)擔(dān)最重的癌癥之一的治療方案。
這些累積下來(lái)的創(chuàng)新也不會(huì)止于HER2低表達(dá)乳腺癌這一新劃分出來(lái)的腫瘤類(lèi)型。在DESTINY-Breast04試驗(yàn)中,HER2表達(dá)最低的蛋白評(píng)分為1的患者與評(píng)分為2的患者療效并無(wú)區(qū)別。這很可能意味著DESTINY-Breast04試驗(yàn)還未觸及對(duì)Trastuzumab Deruxtecan有反應(yīng)的HER2表達(dá)底線。隨著更多更精細(xì)的HER2表達(dá)檢測(cè)方法投入運(yùn)用,或許有更多患者能受益于Trastuzumab Deruxtecan。
2022年12月,F(xiàn)DA根據(jù)Trastuzumab Deruxtecan在非小細(xì)胞肺癌中的臨床試驗(yàn)結(jié)果,又有條件批準(zhǔn)了它在HER2變異的非小細(xì)胞肺癌患者中的使用。從HER2靶向藥的角度看,Trastuzumab Deruxtecan正在實(shí)現(xiàn)只要有HER2表達(dá),不論高低,不論癌癥,都有希望治療的靶點(diǎn)潛力徹底挖掘。而這又是在實(shí)現(xiàn)制藥界長(zhǎng)期以來(lái)對(duì)抗體偶聯(lián)藥的期望:1+1>2,通過(guò)抗體偶聯(lián)的平臺(tái),獲得單獨(dú)的抗體藥或偶聯(lián)的細(xì)胞毒性藥,都無(wú)法做到的治療效果。
Trastuzumab Deruxtecan的成功,也催生了抗體偶聯(lián)藥物的大熱。諸多新一代抗體偶聯(lián)藥物進(jìn)入驗(yàn)證,乃至進(jìn)入市場(chǎng)。在一些偶聯(lián)藥物里,連接的不再只是化學(xué)毒性物質(zhì),例如免疫刺激藥物、放療藥物都有嘗試。當(dāng)然我們很難預(yù)測(cè)這些藥物是否會(huì)成功,可能不少抗體偶聯(lián)藥會(huì)以失敗告終。但隨著技術(shù)的積累,我們或許會(huì)看到越來(lái)越多的患者獲益于這些潛在的創(chuàng)新藥。而假如若干年后,我們回顧抗體偶聯(lián)藥的發(fā)展史,Trastuzumab Deruxtecan很可能就是這一技術(shù)平臺(tái)的轉(zhuǎn)折點(diǎn)。
多方位創(chuàng)新讓有效藥更快與患者見(jiàn)面
除了技術(shù)層面的創(chuàng)新,同樣值得注意的是Trastuzumab Deruxtecan在HER2低表達(dá)人群的獲批從藥企遞交申請(qǐng)到FDA批準(zhǔn)只用了不到兩周的時(shí)間,距離相關(guān)試驗(yàn)結(jié)果公布也不過(guò)兩個(gè)月。這比FDA原定批準(zhǔn)時(shí)間早了近4個(gè)月的提速,背后是藥物監(jiān)管方面的創(chuàng)新。
FDA對(duì)Trastuzumab Deruxtecan的審核采用了實(shí)時(shí)腫瘤藥物審核(Real-Time Oncology Review ,RTOR)與Orbis計(jì)劃。RTOR意味著研發(fā)方可以將有效性與安全性數(shù)據(jù)更早遞交到FDA,讓藥品審核更早開(kāi)始。Oribis計(jì)劃則是讓國(guó)家上多個(gè)藥品監(jiān)管部門(mén)合作,協(xié)同對(duì)藥品的審核過(guò)程,在很多藥物的臨床試驗(yàn)進(jìn)入國(guó)際化的當(dāng)下,加速數(shù)據(jù)的審核與一個(gè)藥品在全球的上市。
各方面的創(chuàng)新意味著我們看到越來(lái)越多的創(chuàng)新藥以越來(lái)越快的速度上市。曲妥珠單抗最早的臨床試驗(yàn)是在1992年,即使采用了加速審批,也是在1998年才被FDA批準(zhǔn)。而Trastuzumab Deruxtecan第一個(gè)臨床試驗(yàn)是在2015年,2019年就獲得第一個(gè)適應(yīng)癥批準(zhǔn),如今更是以驚人的速度擴(kuò)展適用人群。
這些創(chuàng)新在中國(guó)發(fā)生。曲妥珠單抗原研藥2002年批準(zhǔn)在中國(guó)上市,2017年才進(jìn)入醫(yī)保目錄。而Trastuzumab Deruxtecan在2022年5月就被中國(guó)藥監(jiān)局納入優(yōu)先審批行列,距今不到一年就獲批。甚至在藥監(jiān)局審批前,2022年2月就落戶海南博鰲樂(lè)城國(guó)際醫(yī)療旅游先行區(qū)。這次中國(guó)獲批的還是HER2陽(yáng)性乳腺癌,但HER2低表達(dá)乳腺癌的上市申請(qǐng)也已被藥監(jiān)局受理。從Trastuzumab Deruxtecan上,我們可以看到近年來(lái)很多對(duì)患者幫助極大的創(chuàng)新藥的軌跡:國(guó)內(nèi)外上市的時(shí)間差不斷縮短。此外,國(guó)內(nèi)也有大量的抗體偶聯(lián)藥屬于研發(fā)狀態(tài),在技術(shù)層面的創(chuàng)新也在與國(guó)外逐漸同步。
乳腺癌仍然是全球最常見(jiàn)、致死人數(shù)最多的癌癥之一,而癌癥又是全球最致命的疾病類(lèi)型之一,每6例死亡中就有1例是癌癥導(dǎo)致。但我們?nèi)韵M缤琓rastuzumab Deruxtecan正在書(shū)寫(xiě)的乳腺癌治療革新,各個(gè)層面的創(chuàng)新綜合在一起,可以讓癌癥對(duì)我們的威脅,對(duì)社會(huì)的負(fù)擔(dān)不斷下降。
(作者周葉斌,系美國(guó)阿拉巴馬大學(xué)伯明翰分校遺傳性博士,長(zhǎng)期從事免疫學(xué)研究,目前在藥企從事新藥研發(fā)。)
參考資料:
1.https://www.who.int/news-room/fact-sheets/detail/breast-cancer
2.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8330522/
3.https://www.cancer.org/cancer/breast-cancer/understanding-a-breast-cancer-diagnosis/breast-cancer-survival-rates.html
4.https://www.mdpi.com/2072-6694/12/8/2081
5.https://www.herceptin.com/hcp/indications.html
6.https://seer.cancer.gov/statfacts/html/breast-subtypes.html
7.https://www.fda.gov/news-events/press-announcements/fda-approves-new-treatment-option-patients-her2-positive-breast-cancer-who-have-progressed-available
8.https://www.nejm.org/doi/full/10.1056/NEJMoa2203690?query=featured_home
9.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-fam-trastuzumab-deruxtecan-nxki-her2-low-breast-cancer
10.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-gemtuzumab-ozogamicin-cd33-positive-aml
11.https://www.nature.com/articles/s41591-022-01935-8
12.https://www.himd.com/article/r_191_94.html
13.https://www.pharmcube.com/index/news/article/9531
14.https://www.who.int/news-room/fact-sheets/detail/cancer





- 報(bào)料熱線: 021-962866
- 報(bào)料郵箱: news@thepaper.cn
滬公網(wǎng)安備31010602000299號(hào)
互聯(lián)網(wǎng)新聞信息服務(wù)許可證:31120170006
增值電信業(yè)務(wù)經(jīng)營(yíng)許可證:滬B2-2017116
? 2014-2025 上海東方報(bào)業(yè)有限公司




