- +1
還要等十年,mRNA癌癥疫苗研發(fā)難在哪?
原創(chuàng) 轉(zhuǎn)網(wǎng) 轉(zhuǎn)化醫(yī)學(xué)網(wǎng) 收錄于合集 #行業(yè)動(dòng)態(tài) 434個(gè)

在mRNA疫苗之前,美國(guó)FDA在約十年前批準(zhǔn)的首個(gè)癌癥疫苗普列威(Provenge)用于治療前列腺,這是一款由中國(guó)企業(yè)研發(fā)的疫苗。不過(guò)由于這款疫苗并未帶來(lái)顛覆性的療效,僅將晚期患者的生存期延長(zhǎng)了4個(gè)月,未能開(kāi)創(chuàng)癌癥疫苗的新紀(jì)元。

本文為轉(zhuǎn)化醫(yī)學(xué)網(wǎng)原創(chuàng),轉(zhuǎn)載請(qǐng)注明出處
作者:kope
隨著腫瘤治療技術(shù)的提升,治療性癌癥疫苗未來(lái)的應(yīng)用場(chǎng)景可能有限。上海公共衛(wèi)生臨床中心轉(zhuǎn)化醫(yī)學(xué)研究院院長(zhǎng)徐建青表示:“未來(lái)十年腫瘤治療技術(shù)將會(huì)面臨重大的變革,治療性疫苗可能會(huì)因?yàn)槿芰霾《警煼夹g(shù)等的快速發(fā)展而失去一部分價(jià)值,可應(yīng)用的場(chǎng)景也會(huì)受限。”
無(wú)法預(yù)防癌癥
01
疫情期間,新冠疫苗成了抗疫的“終極武器”之一。如今,使用同樣思路的癌癥疫苗可能也將在十年內(nèi)問(wèn)世。針對(duì)癌癥研發(fā)的mRNA疫苗可能無(wú)法在近期內(nèi)取得突破,德國(guó)mRNA疫苗廠商BioNTech公司聯(lián)合創(chuàng)始人吳沙忻(UgurSahin)夫婦周日接受媒體采訪時(shí)稱(chēng),mRNA癌癥疫苗的上市可能要等到2030年左右。
“作為科學(xué)家,我們總是不愿說(shuō)我們將治愈癌癥,但我們還是希望能有一些突破。”BioNTech聯(lián)合創(chuàng)始人zlem Türeci表示。她還說(shuō)道,通過(guò)新冠疫苗的研發(fā)和產(chǎn)業(yè)化,BioNTech已經(jīng)更好地了解了人的免疫系統(tǒng)如何對(duì)mRNA作出反應(yīng),掌握了如何大規(guī)模地制造mRNA疫苗,并與監(jiān)管機(jī)構(gòu)就疫苗批準(zhǔn)相關(guān)事宜進(jìn)行反復(fù)溝通,這些都能夠加速未來(lái)癌癥疫苗的上市。
正在研發(fā)的癌癥疫苗是一種治療性的疫苗,作為一種癌癥治療手段,促使免疫系統(tǒng)破壞癌細(xì)胞,從而預(yù)防腫瘤的復(fù)發(fā)。但癌癥疫苗的研發(fā)難度大,仍需要克服重大挑戰(zhàn)。其中一個(gè)重要挑戰(zhàn)就是由于構(gòu)成腫瘤的癌細(xì)胞中可能含有多種不同的蛋白質(zhì),因此要讓疫苗針對(duì)癌細(xì)胞而不傷害健康組織極為困難。
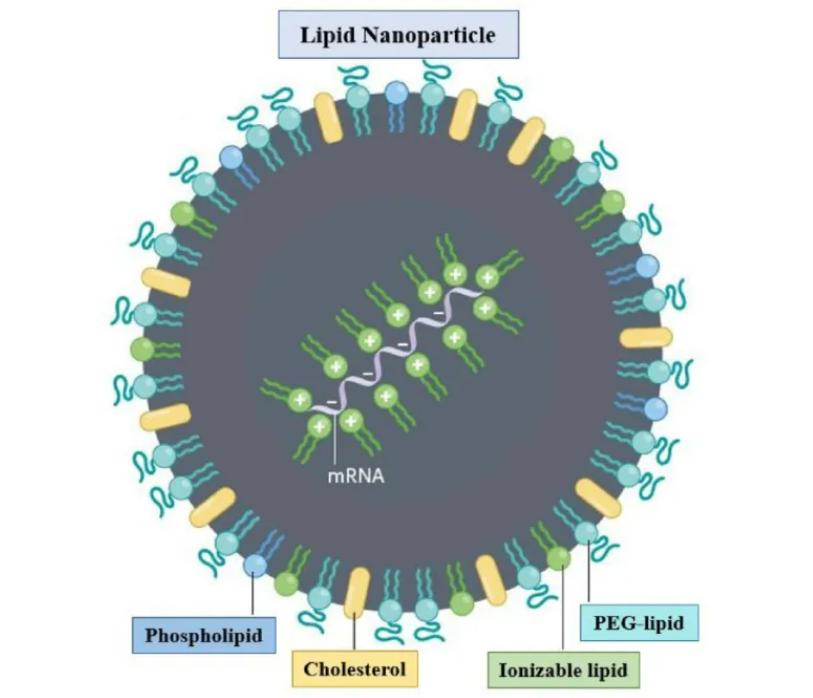
研發(fā)難在哪
02
2021年2月,Molecular Cancer雜志的一篇綜述總結(jié)了mRNA疫苗在腫瘤治療領(lǐng)域的應(yīng)用,已有20多種基于mRNA的免疫療法進(jìn)入臨床試驗(yàn),在實(shí)體瘤治療方面已初見(jiàn)成效。臨床中的腫瘤治療mRNA疫苗可分為三大類(lèi):編碼免疫刺激物的mRNA疫苗、編碼TAAs (腫瘤相關(guān)抗原) 的mRNA疫苗和編碼新抗原 (neoantigens) 的個(gè)性化疫苗。裸mRNA或基于載體的mRNA疫苗能有效地表達(dá)腫瘤抗原,促進(jìn)抗原遞呈細(xì)胞激活并刺激天然/適應(yīng)性免疫。
mRNA指導(dǎo)細(xì)胞生產(chǎn)自身所需蛋白質(zhì),靶點(diǎn)可在細(xì)胞內(nèi)或分泌到細(xì)胞外,因此理論上可將編碼相應(yīng)蛋白質(zhì)的mRNA通過(guò)一定手段運(yùn)送到細(xì)胞質(zhì)內(nèi),從而對(duì)所有蛋白質(zhì)層面疾病發(fā)揮療效。但是由于其大小、電荷和可降解性,裸露的mRNA不容易穿過(guò)細(xì)胞膜并有效滲入到細(xì)胞質(zhì),因此如何將mRNA遞送至細(xì)胞質(zhì)中并及時(shí)指導(dǎo)蛋白質(zhì)生產(chǎn)將成為核心。
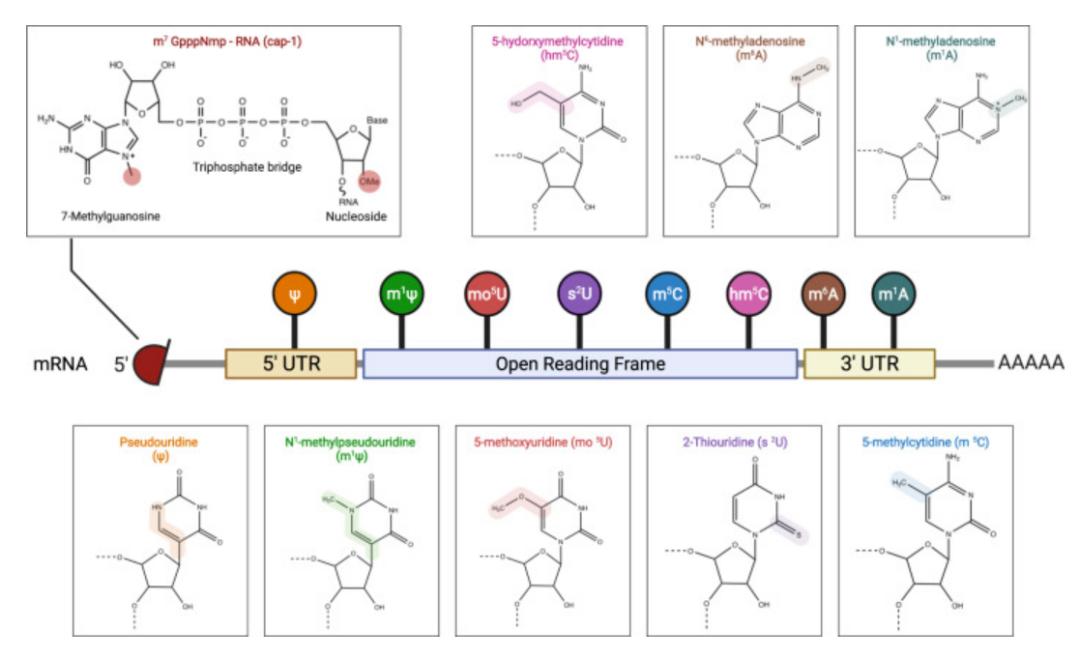
2021年6月CureVac宣布其開(kāi)發(fā)的mRNA疫苗CVnCoV在2b/3期臨床試驗(yàn)中預(yù)防感染COVID-19僅有47%的保護(hù)力,可能失敗的原因包括未對(duì)編碼區(qū)的核苷酸進(jìn)行修飾。mRNA 疫苗生產(chǎn)過(guò)程中會(huì)產(chǎn)生很多雜質(zhì),無(wú)論是在質(zhì)粒生產(chǎn)、純化與線性過(guò)程中,還是在體外轉(zhuǎn)錄、加帽等過(guò)程中,均會(huì)涉及到多步純化與超濾,如何保證上一步工藝不影響下一步工藝尤為重要,同時(shí)需要保證mRNA和遞送系統(tǒng)的穩(wěn)定性。
歷經(jīng)60載
03
mRNA從首次發(fā)現(xiàn)到作為商品銷(xiāo)售大概經(jīng)歷了60年,技術(shù)的發(fā)展經(jīng)歷了以下幾個(gè)階段。
1)1961-1990年:mRNA從理論照進(jìn)現(xiàn)實(shí)。從1961年mRNA的發(fā)現(xiàn),到1990年全球首次發(fā)表小鼠體內(nèi)體外轉(zhuǎn)錄mRNA的報(bào)告,明確了mRNA的具體機(jī)制和作用以及其發(fā)展?jié)摿Α?/p>
2)1990-2009年:分子修飾等關(guān)鍵技術(shù)使得人體應(yīng)用成為可能。從上世紀(jì)90年代到2009年,mRNA技術(shù)實(shí)現(xiàn)了從動(dòng)物到人體的突破,2005年發(fā)現(xiàn)化學(xué)修飾可降低mRNA免疫原性,2009年首次在人體上應(yīng)用癌癥免疫治療。
3)2009-2022年:遞送技術(shù)的發(fā)展推動(dòng)人體臨床大規(guī)模開(kāi)展。2009年脂質(zhì)納米顆粒 (LNP) 遞送系統(tǒng)首次申請(qǐng)專(zhuān)利。2015年首個(gè)LNP遞送技術(shù)以及序列修飾技術(shù)的逐漸成熟,給mRNA行業(yè)發(fā)展帶來(lái)充足的動(dòng)力,多項(xiàng)mRNA疫苗開(kāi)展臨床。
4)2020年-至今:商業(yè)化時(shí)代正式開(kāi)啟,2020年全球首個(gè)mRNA商業(yè)化產(chǎn)品上市,迅速得到資本市場(chǎng)的追捧。
參考資料:
https://www.cn-healthcare.com/articlewm/20220527/content-1364221.html
https://baijiahao.baidu.com/s?id=1746928889196889072&wfr=spider&for=pc
注:本文旨在介紹醫(yī)學(xué)研究進(jìn)展,不能作為治療方案參考。如需獲得健康指導(dǎo),請(qǐng)至正規(guī)醫(yī)院就診。
本文為澎湃號(hào)作者或機(jī)構(gòu)在澎湃新聞上傳并發(fā)布,僅代表該作者或機(jī)構(gòu)觀點(diǎn),不代表澎湃新聞的觀點(diǎn)或立場(chǎng),澎湃新聞僅提供信息發(fā)布平臺(tái)。申請(qǐng)澎湃號(hào)請(qǐng)用電腦訪問(wèn)http://renzheng.thepaper.cn。





- 報(bào)料熱線: 021-962866
- 報(bào)料郵箱: news@thepaper.cn
滬公網(wǎng)安備31010602000299號(hào)
互聯(lián)網(wǎng)新聞信息服務(wù)許可證:31120170006
增值電信業(yè)務(wù)經(jīng)營(yíng)許可證:滬B2-2017116
? 2014-2025 上海東方報(bào)業(yè)有限公司




